题目内容
下列说法正确的是
| A.单质铯的熔点比单质锂的高 |
| B.胶体的胶粒不能通过滤纸 |
| C.元素N的氢化物的沸点比元素P的氢化物的沸点低 |
| D.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌 |
D
解析试题分析:A、碱金属元素单质的熔点自上而下逐渐降低,所以铯的熔点比锂的低,错误;B、胶体的胶粒可以透过滤纸,不能透过半透膜,错误;C、氨气的分子间可以形成氢键,所以元素N的氢化物的沸点比元素P的氢化物的沸点高,错误;D、锌片作阳极,则Zn失去电子生成Zn2+,所以电解氯化锌溶液,在阴极铁极有Zn析出,正确,答案选D。
考点:考查同主族元素的性质,胶体的性质,电解原理的应用

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案某次实验需用0.4 mol/L NaOH溶液480 mL。配制方法如下:
(1)配制该溶液应选用_______________mL容量瓶;
(2)用托盘天平准确称量__________g 固体NaOH;
(3)将称量好的NaOH固体放在500 mL大烧杯中,倒入约300 mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待__________________后,将烧杯中的溶液注入容量瓶中;用少量蒸馏水洗涤烧杯 次,洗涤后的溶液一并转入容量瓶,轻轻晃动容量瓶,使溶液混合均匀;向容量瓶中加入蒸馏水,到液面_____________________时,改用__________加蒸馏水至液面最低点与刻度线相切。盖好瓶塞,上下颠倒混合均匀;若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是___________,偏低的是___________,对实验结果没有影响的是___________(填各选项的序号)。
| A.所用的NaOH中混有少量Na2O |
| B.用托盘天平称量一定质量固体NaOH时,所用的小烧杯内壁不太干燥 |
| C.配制溶液所用的容量瓶洗净后没有烘干 |
| D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作 |
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线。
如图表示一些物质间的从属关系,不正确的是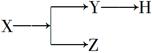
| | X | Y | Z | H |
| A | 分散系 | 胶体 | 溶液 | 烟 |
| B | 元素周期表的纵行 | 主族 | 副族 | 卤族 |
| C | 电解质 | 酸 | 碱 | 盐 |
| D | 化合物 | 共价化合物 | 离子化合物 | 酸 |
下列有关概念说法正确的是
| A.D2、T2、H2互为同素异形体 |
| B.甲烷和异丁烷互为同系物 |
| C.石墨、金刚石互为同位素 |
| D.乙烷和乙烯互为同分异构体 |
酸碱质子理论认为,凡是能给出质子(H+)的都是酸,凡能结合质子的都是碱,依据酸碱质子理论属于酸碱两性物质的是
| A.HCl | B.NaOH |
| C.Fe2O3 | D.NaHCO3 |
Fe(OH)3胶体虽然是由FeCl3溶液制得,但两者是截然不同的两种物质。FeCl3溶液、Fe(OH)3胶体共同具备的性质是
| A.都呈透明的红褐色 | B.都比较稳定,密封保存一段时间都不会产生沉淀 |
| C.分散质颗粒直径相同 | D.当有光线透过时,都能产生丁达尔效应 |
下列物质属于纯净物的是
| A.冰水混合物 | B.无污染的空气 | C.盐酸 | D.漂白粉 |
人们用DNA制造出一种臂长只有7nm的纳米镊子,这种镊子能钳起分子或原子,并对它随意组合。下列分散系中,分散质微粒直径与纳米粒具有相同数量级的是
| A.溶液 | B.胶体 | C.悬浊液 | D.乳浊液 |