题目内容
10.扁桃酸衍生物是重要的医药中间体,以A和B为原料合成扁桃酸衍生物F的路线如图1: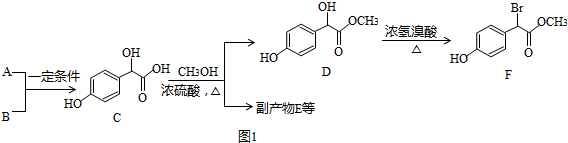
(1)A分子式为C2H2O3,可发生银镜反应,且具有酸性,A所含官能团名称为醛基、羧基,写出A+B→C的化学反应方程式:
 ;
;(2)C(
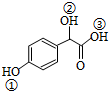 )中①、②、③3个-OH的酸性由强到弱的顺序是③>①>②;
)中①、②、③3个-OH的酸性由强到弱的顺序是③>①>②;(3)E是由2分子C生成的含有3个六元环的化合物,E分子中不同化学环境的氢原子有4种.
(4)D→F的反应类型是取代反应,1molF在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为3mol.
写出符合下列条件的F的所有同分异构体(不考虑立体异构)的结构简式:
 .
.①属于一元酸类化合物
②苯环上只有2个取代基且处于对位,其中一个是羟基
(5)已知:
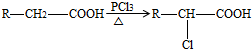
A有多种合成方法,在图2方框中写出由乙酸合成A的路线流程图(其他原料任选),合成路线流程图示例如下:H2C=CH2$→_{催化剂,△}^{H_{2}O}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOC2H5.

分析 (1)A的分子式为C2H2O3,可发生银镜反应,且具有酸性,含有醛基和羧基,则A是OHC-COOH,根据C的结构可知B是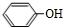 ,A+B→C发生加成反应;
,A+B→C发生加成反应;
(2)羧基的酸性强于酚羟基,酚羟基的酸性强于醇羟基;
(3)C中有羟基和羧基,2分子C可以发生酯化反应,可以生成3个六元环的化合物,C分子间醇羟基、羧基发生酯化反应,则E为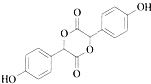 ;
;
(4)对比D、F的结构,可知溴原子取代-OH位置;F中溴原子、酚羟基、酯基(羧酸与醇形成的酯基),都可以与氢氧化钠反应;
F的所有同分异构体符合:①属于一元酸类化合物,②苯环上只有2个取代基且处于对位,其中一个是羟基,另外取代基为-CBr(CH3)COOH、-CH(CH2Br)COOH、-CH2CHBrCOOH、-CHBrCH2COOH;
(5)由题目信息可知,乙酸与PCl3反应得到ClCH2COOH,在氢氧化钠水溶液、加热条件下发生水解反应得到HOCH2COONa,用盐酸酸化得到HOCH2COOH,最后在Cu作催化剂条件下发生催化氧化得到OHC-COOH.
解答 解:(1)A的分子式为C2H2O3,可发生银镜反应,且具有酸性,含有醛基和羧基,则A是OHC-COOH,根据C的结构可知B是 ,A+B→C发生加成反应,反应方程式为:
,A+B→C发生加成反应,反应方程式为: ,
,
故答案为:醛基、羧基; ;
;
(2)羧基的酸性强于酚羟基,酚羟基的酸性强于醇羟基,故强弱顺序为:③>①>②,
故答案为:③>①>②;
羧基的酸性强于酚羟基,酚羟基的酸性强于醇羟基;
(3)C中有羟基和羧基,2分子C可以发生酯化反应,可以生成3个六元环的化合物,C分子间醇羟基、羧基发生酯化反应,则E为 ,为对称结构,分子中有4种化学环境不同的H原子,分别为苯环上2种、酚羟基中1种、亚甲基上1种,
,为对称结构,分子中有4种化学环境不同的H原子,分别为苯环上2种、酚羟基中1种、亚甲基上1种,
故答案为:4;
(4)对比D、F的结构,可知溴原子取代-OH位置,D→F的反应类型是:取代反应;F中溴原子、酚羟基、酯基(羧酸与醇形成的酯基),都可以与氢氧化钠反应,1molF最多消耗3mol NaOH;
F的所有同分异构体符合:①属于一元酸类化合物,②苯环上只有2个取代基且处于对位,其中一个是羟基,另外取代基为-CBr(CH3)COOH、-CH(CH2Br)COOH、-CH2CHBrCOOH、-CHBrCH2COOH,可能的结构简式为: ,
,
故答案为:取代反应;3; ;
;
(5)由题目信息可知,乙酸与PCl3反应得到ClCH2COOH,在氢氧化钠水溶液、加热条件下发生水解反应得到HOCH2COONa,用盐酸酸化得到HOCH2COOH,最后在Cu作催化剂条件下发生催化氧化得到OHC-COOH,合成路线流程图为:CH3COOH$→_{△}^{PCl_{3}}$ClCH2COOH$→_{△}^{NaOH/H_{2}O}$HOCH2COONa$\stackrel{HCl}{→}$HOCH2COOH$→_{△}^{O_{2}/Cu}$OHC-COOH,
故答案为:CH3COOH$→_{△}^{PCl_{3}}$ClCH2COOH$→_{△}^{NaOH/H_{2}O}$HOCH2COONa$\stackrel{HCl}{→}$HOCH2COOH$→_{△}^{O_{2}/Cu}$OHC-COOH.
点评 本题考查有机物的推断与合成、同分异构体的书写、常见有机反应类型、官能团的性质等,是对有机化学基础的综合考查,难度中等.

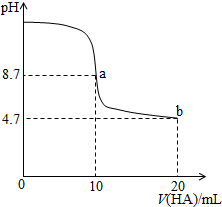
| A. | a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA) | |
| B. | a、b两点所示溶液中水的电离程度相同 | |
| C. | pH=7时,c(Na+)=c(A-)+c(HA) | |
| D. | b点所示溶液中c(A-)>c(HA) |
| A. | 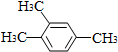 1,2,4-三甲苯 | B. | 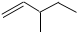 3-甲基戊烯 | C. | 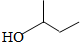 2-甲基-1-丙醇 | D. |  1,3-二溴丙烷 |
| A. | 在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ | |
| B. | 气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气 | |
| C. | 灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+ | |
| D. | 将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2 |
| A. | 分子式为C2H6O的有机化合物性质相同 | |
| B. | 相同条件下,等质量的碳按a、b两种途径完全转化,途径a比途径b放出更多热能 途径a:C$→_{高温}^{H_{2}O}$CO+H2$→_{燃烧}^{O_{2}}$CO2+H2O 途径b:C$→_{燃烧}^{O_{2}}$CO2 | |
| C. | 在氧化还原反应中,还原剂失去电子总数等于氧化剂得到电子的总数 | |
| D. | 通过化学变化可以直接将水转变为汽油 |
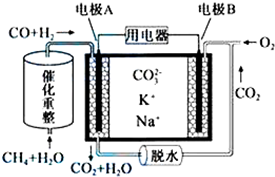
| A. | 反应CH4+H2O$\frac{\underline{催化剂}}{△}$3H2+CO,每消耗1molCH4转移12mol电子 | |
| B. | 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
| A. | LiAlH4中H元素的化合价为-1 | |
| B. | LiAlH4L、iAlO2、LiH均是离子化合物 | |
| C. | 1mol LiAlH4在125℃完全分解,转移4mol电子 | |
| D. | 0.5 mol LiAlH4与水充分反应后产生44.8L H2 |
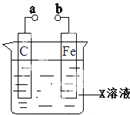
| A. | X如果是硫酸铜,a和b分别连接直流电源正、负极,一段时间后铁片质量增加 | |
| B. | X如果是氯化钠,则a和b连接时,该装置可模拟生铁在食盐水中被腐蚀的过程 | |
| C. | X如果是硫酸铁,则不论a和b是否用导线连接,铁片均发生氧化反应 | |
| D. | X如果是氢氧化钠,将碳电极改为铝电极,a和b用导线连接,此时构成原电池铁作负极 |