题目内容
【题目】A、B、C是中学化学中常见的三种元素(A、B、C代表元素符号)。A位于元素周期表中第四周期,其基态原子最外层电子数为2,且内层轨道全部排满电子。短周期元素B的一种常见单质为淡黄色粉末。元素C的原子最外层电子数是其内层电子数的3倍。
(1)在第三周期中,第一电离能大于B的元素有____种。
(2)B的氢化物(H2B)分子的立体构型为____,C的氢化物H2C、H2C2中C的杂化类型分别是________、____,在乙醇中的溶解度:S(H2C)>S(H2B),其原因是____。
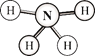
(3)A的氯化物与氨水反应可形成配合物[A(NH3)4]Cl2,1mol该配合物中含有σ键的物质的量为____mol。
【答案】3 V形(或角形) sp3 sp3 水分子与乙醇分子之间形成氢键 16
【解析】
A、B、C是中学化学中常见的三种元素,A位于元素周期表中第4周期,其基态原子最外层电子数为2,且内层轨道全部排满电子,核外电子排布为1s22s22p63s23p63d104s2,为Zn元素;短周期元素B的一种常见单质为淡黄色粉末,则B为S元素;C的原子最外层电子数是其内层电子数的3倍,C原子只能有2个电子层,最外层电子数为6,则C为O元素,据此分析解答。
根据上述分析,A为Zn元素,B为S元素,C为O元素。
(1)在第3周期中,第一电离能大于S的元素有P、Cl、Ar,故答案为:3;
(2)H2S分子中S原子的价层电子对数为2+![]() =4,S原子有2对孤电子对,故其空间构型为V型;C的氢化物H2O、H2O2中O原子的价层电子对数分别为2+
=4,S原子有2对孤电子对,故其空间构型为V型;C的氢化物H2O、H2O2中O原子的价层电子对数分别为2+![]() =4,3+
=4,3+![]() =4,杂化类型分别都是sp3杂化;水分子与乙醇分子之间能够形成氢键,故在乙醇中的溶解度:S(H2O)>S(H2S),故答案为:V型;sp3;sp3;水分子与乙醇分子之间形成氢键;
=4,杂化类型分别都是sp3杂化;水分子与乙醇分子之间能够形成氢键,故在乙醇中的溶解度:S(H2O)>S(H2S),故答案为:V型;sp3;sp3;水分子与乙醇分子之间形成氢键;
(3)Zn的氯化物与氨水反应可形成配合物[Zn(NH3)4]Cl2,[Zn(NH3)4]2+中含有12个N-H键、4个配位键,故含有16个σ键,则1mol该配合物中含有σ键的物质的量为16mol,故答案为:16。

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】![]() 、
、![]() 、
、![]() 、
、![]() 是四种短周期元素,它们的核电荷数依次增大,四种元素的性质或原子结构的部分信息如表所示。
是四种短周期元素,它们的核电荷数依次增大,四种元素的性质或原子结构的部分信息如表所示。
元素 | 元素性质或原子结构的部分信息 |
| 元素的离子核外无电子 |
| 地壳中含量最多的元素 |
| 元素的离子半径在该周期中最小 |
|
|
下列叙述不正确的是( )
A.![]() 与
与![]() 形成的化合物在常温下为气体
形成的化合物在常温下为气体
B.![]() 的最高价氧化物对应的水化物不与
的最高价氧化物对应的水化物不与![]() 溶液反应
溶液反应
C.![]() 和
和![]() 形成的常见化合物能形成酸雨
形成的常见化合物能形成酸雨
D.简单氢化物的稳定性:![]()
【题目】根据下表回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ |
(1)写出下列元素符号:①______,⑥______,⑦______,⑨______。
(2)在这些元素中,最活泼的金属元素是______(填元素符号,下同),最活泼的非金属元素是______,最不活泼的元素是______。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是__________________,碱性最强的是__________________,呈两性的氢氧化物是__________________;三者之间相互反应的化学方程式是____________________________________。
(4)在这些元素(稀有气体元素除外)中,原子半径最小的是__________,原子半径最大的是____。
(5)在③与④中,化学性质较活泼的是__________,怎样用化学实验证明?______________ 在⑧与中,化学性质较活泼的是______,怎样用化学实验证明?________________________。