��Ŀ����
����Ŀ���������ƣ�NaNO2����ۿ���ʳ��������ζ����һ�ֳ��õķ�ɫ���ͷ�������ʹ�ù�����ʹ���ж��������϶�ʳƷ���������Ƶ����������ںܵ͵�ˮƽ�ϡ�ijѧϰС����������������������ʵ�飺
��ʵ��I���Ʊ�NaNO2
��С���������֪��2NO+Na2O2=2NaNO2�� 2NO2+Na2O2=2NaNO3
����Ʊ�װ�����£��г�װ����ȥ����
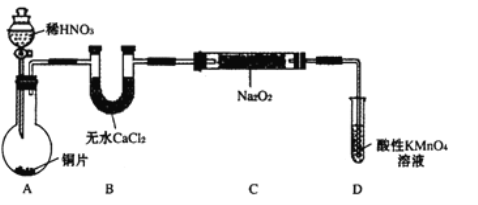
��1��װ��D�ɽ�ʣ���NO������NO3-��������Ӧ�����ӷ���ʽΪ ��
��2�����û��Bװ�ã�C�з����ĸ���Ӧ�� , ��
��3����ͬѧ�����װ�����������ú����ʵ�飬�����Ƶõ�NaNO2�����н϶��NaNO3���ʡ�������A��Bװ�ü������� װ�����Ľ��������NaNO2�Ĵ��ȡ�
��ʵ�������ⶨ��ȡ����Ʒ��NaNO2�ĺ���
���裺
a����5���б�ŵĴ��̶��Թܣ���ɫ�ܣ��зֱ���벻ͬ����NaNO2��Һ��������1 mL��M��Һ��M��NaNO2���Ϻ�ɫ��NaNO2Ũ��Խ����ɫԽ����ټ�����ˮ���������Ϊ10 mL�����Ƴɱ�ɫ�ף�
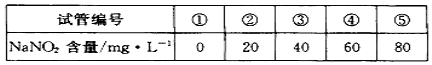
b������0��10 g�Ƶõ���Ʒ����ˮ���500 mL��Һ��ȡ5 mL����Һ������1 mL M��Һ���������ˮ��10 mL�����ɫ�ױȽϡ�
��4������b�бȽϽ���ǣ�����Һ��ɫ������ɫ����ͬ�����ͬѧ�Ƶõ���Ʒ��NaNO2������������ %��
��5����Ŀ�ӱ�ɫ��֤��ά����C������Ч����NaNO2�ĺ�������Ʋ��������ʵ�鱨�档
ʵ�鷽�� | ʵ������ | ʵ����� |
ȡ5mL����Һ���� �����ټ���1ml M��Һ �� ������������ɫ�Աȡ� | ά����C������Ч����NaNO2 �ĺ����� |
���𰸡���1��5NO+3MnO4-+4H+��5NO3-+3Mn2++2H2O��
��2��2Na2O2+2H2O��4NaOH+O2����2NO+O2��NO2��
��3��װ��ˮ��ϴ��ƿ��
��4��40��
��5��ά����C����������ˮ��10mL���Ϻ�ɫ����ɫ��dz��
��������
�����������1��NO������2����5��3��KMnO4��Mn����7����2��5����С��������15��������ӷ�Ӧ����ʽΪ5NO��3MnO4����4H��=5NO3����3Mn2����2H2O��
��2��Bװ�õ���������NO�е�ˮ���������û��Bװ����NO�л���ˮ������2Na2O2��2H2O=4NaOH��O2����2NO��O2=2NO2��
��3��������Ŀ����Ϣ��NaNO3����NO2�������Ʒ�Ӧ���ɵ��������Ҫ��ȥNO2��3NO2��H2O=2HNO3��NO�����A��B֮��װ��ˮ��ϴ��ƿ��
��4�����ݱ�ɫ�ף�NaNO2������������40%��
��5��ά����C����������ˮ��10mL����ΪNaNO2Ũ��Խ����ɫԽ������Һ��ɫ�Ϻ�ɫ�Ȣ�ɫ��dz��

 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�