题目内容
【题目】将2.32g碳酸钠、氢氧化钠的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中正确的是( )
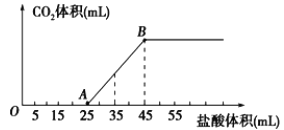
A.OA段发生反应的离子方程式为:H++OH-→H2O
B.B当加入35mL盐酸时,产生CO2的体积为224mL
C.A点溶液中的溶质为NaC1、Na2CO3
D.混合物中NaOH的质量0.60g
【答案】B
【解析】
A、根据图像,OA段没有二氧化碳气体放出,发生反应的离子方程式为:H++OH-═H2OCO32-+H+═HCO3-,故A错误;
B、AB段反应放出二氧化碳,发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,根据方程式n(CO2)=(35-25)×10-3L×1mol/L=0.01mol,所以二氧化碳的体积为:0.01mol×22.4L/mol=224mL,故B正确;
C、OA段发生反应的离子方程式为:H++OH-═H2OCO32-+H+═HCO3-,所以A点的溶质为NaC1、NaHCO3,故C错误;
D、由反应HCO3-+H+=H2O+CO2↑,n(CO2)=n(Na2CO3)=(45-25)×10-3×1=0.02mol,所以氢氧化钠的质量为2.32g-0.02×106g=0.2g,故D错误;
故选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目