题目内容
5.氨水的碱性较弱,其原因是( )| A. | 它能使酚酞试液变红色 | |
| B. | 氨水极易挥发出氨 | |
| C. | 氨与水结合生成的一水合氨(NH3•H2O)只有小部分电离成NH4+和OH- | |
| D. | 溶于水的氨大部分以NH3分子形式存在 |
分析 溶液碱性和氢氧根离子浓度有关,氨与水结合生成一水合氨(NH3•H2O),氨水溶液中存在一水合氨的电离平衡,由于NH3•H2O为弱碱,只有小部分电离成NH4+和OH-.
解答 解:A、使酚酞试液变红色说明显碱性,不能说明碱性较弱,故A不符合;
B、溶液碱性强弱和氢氧根离子浓度有关,氨水极易挥发出氨,与溶液的碱性较弱无关,故B不符合;
C、溶液碱性和氢氧根离子浓度有关,氨与水结合生成的一水合氨(NH3•H2O),由于NH3•H2O为弱碱,只有小部分电离成NH4+和OH-,所以碱性较弱,故C符合;
D、溶于水的氨大部分以NH3分子存在,说明小部分氨气与水反应生成一水合氨(NH3•H2O),与溶液的碱性较弱无关,故D不符合;
故选C.
点评 本题考查了弱电解质的电离平衡分析,溶液酸碱性的实质分析,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下列各组均有两种有机物,若分别取相同的物质的量,在足量的氧气中完全燃烧,两种有机物耗氧量不相同的是( )
| A. | 乙烯和乙醇 | B. | 苯酚和苯甲醇 | C. | 甲烷和乙酸 | D. | 乙炔和乙醛 |
16.由下列实验事实得出的结论正确的是( )
| 实验事实 | 结论 | |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | 将SO2通入Ba(NO3)2溶液,有白色沉淀生成 | BaSO3难溶于硝酸 |
| C | Na2SiO3溶液中通CO2气体出现浑浊 | 酸性:H2SiO3<H2CO3 |
| D | 浓硫酸使蔗糖变黑 | 浓硫酸有脱水性 |
| A. | A | B. | B | C. | C | D. | D |
13. 工业上可利用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下所示:
工业上可利用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下所示:
请回答下列问题:
(1)反应②是吸热(填“吸热”或“放热”)反应.
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1•K2(用K1、K2表示).
(3)500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”、“=”或“<”).
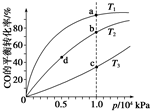
(4)反应①按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是CD(填序号).
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c),v(b)>v(d)
C.平衡常数:K(a)>K(c),K(b)=K(d)
D.平均摩尔质量:M(a)>M(c),M(b)>M(d)
 工业上可利用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下所示:
工业上可利用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下所示:| 化学反应 | 平衡 常数 | 温度/℃ | ||
| 500 | 700 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.34 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 1.70 | 2.52 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | |||
(1)反应②是吸热(填“吸热”或“放热”)反应.
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1•K2(用K1、K2表示).
(3)500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”、“=”或“<”).
(4)反应①按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是CD(填序号).
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c),v(b)>v(d)
C.平衡常数:K(a)>K(c),K(b)=K(d)
D.平均摩尔质量:M(a)>M(c),M(b)>M(d)
20.铝制器皿能够盛放的物质是( )
| A. | 稀硝酸 | B. | 浓硫酸 | C. | NaOH溶液 | D. | 稀硫酸 |
10.下列关于元素周期表的说法正确的是( )
| A. | 元素周期表共有七个周期 | |
| B. | 元素周期表共有18个族 | |
| C. | 所含元素种数最多的族是 VIII族 | |
| D. | 第三周期元素的原子核外都有三个电子层 |
17.填写除去下列物质中的少量杂质(括号内为杂质),所用的试剂和操作方法
| 序号 | 待测物质 | 加入试剂 | 操作方法 |
| ① | 乙醛(乙酸) | NaOH溶液 | |
| ② | CH3CH2OH(水) | ||
| ③ | 苯(苯酚) | ||
| ④ | 乙酸乙酯(乙酸) |
14.设NA代表阿伏伽德罗常数,些列说法正确的是( )
| A. | 42g C3H6中含有的共用电子对数目为8NA | |
| B. | 2g CaCO3和8g KHCO3组成的混合物中碳原子数为0.1 NA | |
| C. | 标准状况下,22.4L氦气与22.4L氟气所含原子数均为2NA | |
| D. | 1L 0.01mol•L-1 KAl(SO4)2溶液中含有的阳离子数目为0.02 NA |
10.常温下,在下列指定条件的各溶液中,一定能大量共存的离子组是( )
| A. | 含0.1 mol.L-1SO2的溶液.中:Na+、Ba2+、Br-、Cl- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、Mg2+、N03-、SO42- | |
| C. | $\frac{C{(H}^{+})}{C({OH}^{-})}$=10-12的溶液中:K+、NH4+、SO42-、NO3- | |
| D. | 不能使酚酞变红的无色溶液中:Na+、K+、ClO-、I- |