题目内容
将3.48g四氧化三铁完全溶解在100ml、1mol/L的硫酸中,然后加入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,则K2Cr2O7的物质的量浓度为 mol/L.
【答案】分析:四氧化三铁中+2铁占 ,3.48g四氧化三铁为0.015mol,完全溶解后溶液中含有Fe2+为0.015mol,入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,令K2Cr2O7的物质的量浓度为cmol/L,表示出Cr2O72-物质的量,根据电子转移守恒列方程计算c的值.
,3.48g四氧化三铁为0.015mol,完全溶解后溶液中含有Fe2+为0.015mol,入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,令K2Cr2O7的物质的量浓度为cmol/L,表示出Cr2O72-物质的量,根据电子转移守恒列方程计算c的值.
解答:解:四氧化三铁中+2铁占 ,3.48g四氧化三铁物质的量为
,3.48g四氧化三铁物质的量为 =0.015mol,
=0.015mol,
所以完全溶解后溶液中含有Fe2+为0.015mol×3× =0.015mol,加入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,令K2Cr2O7的物质的量浓度为cmol/L,则:
=0.015mol,加入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,令K2Cr2O7的物质的量浓度为cmol/L,则:
25×10-3L×cmol/L×2×(6-3)=0.015mol×1
解得:c=0.1
故答案为:0.1.
点评:考查氧化还原反应的计算,难度中等,涉及两步反应,利用方程式计算比较麻烦,关键抓住氧化还原反应中电子转移守恒计算.
 ,3.48g四氧化三铁为0.015mol,完全溶解后溶液中含有Fe2+为0.015mol,入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,令K2Cr2O7的物质的量浓度为cmol/L,表示出Cr2O72-物质的量,根据电子转移守恒列方程计算c的值.
,3.48g四氧化三铁为0.015mol,完全溶解后溶液中含有Fe2+为0.015mol,入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,令K2Cr2O7的物质的量浓度为cmol/L,表示出Cr2O72-物质的量,根据电子转移守恒列方程计算c的值.解答:解:四氧化三铁中+2铁占
 ,3.48g四氧化三铁物质的量为
,3.48g四氧化三铁物质的量为 =0.015mol,
=0.015mol,所以完全溶解后溶液中含有Fe2+为0.015mol×3×
 =0.015mol,加入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,令K2Cr2O7的物质的量浓度为cmol/L,则:
=0.015mol,加入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,令K2Cr2O7的物质的量浓度为cmol/L,则:25×10-3L×cmol/L×2×(6-3)=0.015mol×1
解得:c=0.1
故答案为:0.1.
点评:考查氧化还原反应的计算,难度中等,涉及两步反应,利用方程式计算比较麻烦,关键抓住氧化还原反应中电子转移守恒计算.

练习册系列答案
相关题目
将3.48g四氧化三铁完全溶解在100mL 1mol·L-1硫酸中,然后加入K2Cr2O7溶液25 mL,恰好使溶液中Fe2+全部转化为Fe3+,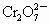 离子全部还原为Cr3+,则K2Cr2O7溶液的物质的量浓度为
离子全部还原为Cr3+,则K2Cr2O7溶液的物质的量浓度为
[ ]
|
A.0.05mol·L-1 |
B.0.1mol·L-1 |
|
C.0.2mol·L-1 |
D.0.3mol·L-1 |