题目内容
A、B、C、D、E是相邻三个周期中的五种元素,它们的原子序数依次增大,B、C、D属同一周期,A、E在周期表中处于同一纵行.已知:①除A外,各元素原子的内层均已填满电子,其中B的最外层有4个电子;②A与B,B与C都能形成共价化合物且常温下为气态;③D与E生成离子化合物,其离子的电子层结构相同.回答:
(1)A为
(2)C元素在周期表中属第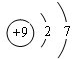
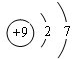 ;
;
(3)D与B形成的化合物的电子式为
 ,属
,属
(4)C与E形成的化合物的电子式为
 和
和
 ,属
,属
(1)A为
氢
氢
元素(填名称,下同),B为碳
碳
元素,C为氧
氧
元素,D为氟
氟
元素,E为钠
钠
元素;(2)C元素在周期表中属第
二
二
周期,ⅦA
ⅦA
族元素,原子的结构示意图为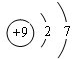
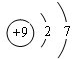
(3)D与B形成的化合物的电子式为


分子
分子
晶体;(4)C与E形成的化合物的电子式为




离子
离子
晶体.分析:A、B、C、D、E是相邻三个周期中的五种元素,它们的原子序数依次增大,除A外,各元素原子的内层均已填满电子,其中B的最外层有4个电子,则B处于ⅣA族,A为H元素或处于过渡元素中,A与B能形成共价化合物且常温下为气态,则可判定A一定为氢,因为如果A是金属,不能与ⅣA族元素形成气态氢化物;B、C、D属同一周期,A、E在周期表中处于同一纵行,由于元素处于相邻三个周期,则B、C、D处于第二周期,E的原子序数最大,则E处于第三周期,故B为碳元素、E为Na元素;B与C都能形成共价化合物且常温下为气态,则C为氧元素,故D为F元素,D与E生成离子化合物,其离子的电子层结构相同,符合题意,据此解答.
解答:解:A、B、C、D、E是相邻三个周期中的五种元素,它们的原子序数依次增大,除A外,各元素原子的内层均已填满电子,其中B的最外层有4个电子,则B处于ⅣA族,A为H元素或处于过渡元素中,A与B能形成共价化合物且常温下为气态,则可判定A一定为氢,因为如果A是金属,不能与ⅣA族元素形成气态氢化物;B、C、D属同一周期,A、E在周期表中处于同一纵行,由于元素处于相邻三个周期,则B、C、D处于第二周期,E的原子序数最大,则E处于第三周期,故B为碳元素、E为Na元素;B与C都能形成共价化合物且常温下为气态,则C为氧元素,故D为F元素,D与E生成离子化合物,其离子的电子层结构相同,符合题意,
(1)由上述分析可知,A为氢元素,B为碳元素,C为氧元素,D为氟元素,E为钠元素,
故答案为:氢;碳;氧;氟;钠;
(2)C氟元素,在周期表中属第二周期ⅦA族,原子的结构示意图为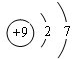 ,
,
故答案为:;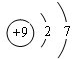 ;
;
(3)D与B形成的化合物为CF4,电子式为 ,属于分子晶体;
,属于分子晶体;
故答案为: ;分子;
;分子;
(4)C与E形成的化合物为Na2O和Na2O2,电子式分别为 和
和 ,都属于离子晶体,
,都属于离子晶体,
故答案为: ;
; ;离子.
;离子.
(1)由上述分析可知,A为氢元素,B为碳元素,C为氧元素,D为氟元素,E为钠元素,
故答案为:氢;碳;氧;氟;钠;
(2)C氟元素,在周期表中属第二周期ⅦA族,原子的结构示意图为
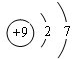 ,
,故答案为:;
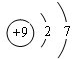 ;
;(3)D与B形成的化合物为CF4,电子式为
 ,属于分子晶体;
,属于分子晶体;故答案为:
 ;分子;
;分子;(4)C与E形成的化合物为Na2O和Na2O2,电子式分别为
 和
和 ,都属于离子晶体,
,都属于离子晶体,故答案为:
 ;
; ;离子.
;离子.点评:本题考查元素推断、电子式等常用化学用语等,难度中等,推断元素是解题关键,确定B处于ⅣA结合A的能与B形成气态分子推断A为氢元素是推断的突破口.

练习册系列答案
相关题目
已知A、B、C、D、E是短周期原子序数依次增大的五种元素,A原子在元素周期表中原子半径最小,B与E同主族,且E的原子序数是B的两倍,C、D是金属,它们的氢氧化物均难溶于水.下列说法不正确的是( )
| A、简单离子的半径:C>D>E>B | B、工业上常用电解法制得C和D的单质 | C、稳定性:A2B>A2E | D、单质D可用于冶炼某些难熔金属 |

 2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
