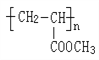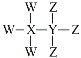题目内容
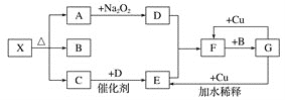
【题目】下图是某些有机物之间的转化关系图:
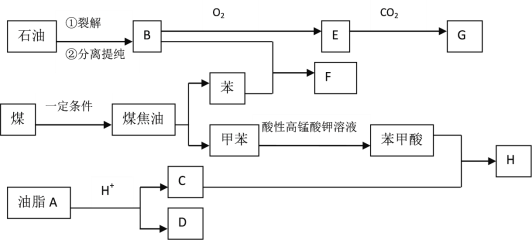
已知:①油脂A的分子式为C57H104O6,且反应生成C、D的物质的量之比为1: 3
②E的分子式为C3H6O,含有甲基且所有碳原子都是饱和碳原子
③G是一种可降解高聚物,其化学式可表示为![]()
试回答下列问题:
(1)G中官能团的名称是_______,D的分子式为_____________,E的结构简式为____________。
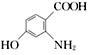
(2)下列关于苯甲酸说法正确的是_______
A 其结构式为![]()
B 其苯环上的一氯代物有3种
C 1个分子可与4个氢气分子发生加成反应
D 与图中有机物C反应可得到5种不同的酯类物质(不考虑立体异构)
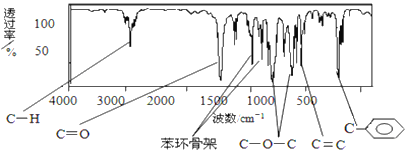
(3)烃B与苯在一定条件下1:1反应生成F,分析F的1H核磁共振谱图,共有5个吸收峰,且峰面积之比为1:1:2:2:6,写出B与苯反应生成F的化学方程式:____________________________。
(4)写出所有符合下列要求的E的同分异构体(不包括E):_________________________________。
①链状化合物 ②氢谱上只有3组峰 ③分子中不含C=C—OH结构
(5)现有甲苯与C的混合液体,其含碳量为60%。取92g该混合液体完全燃烧,将产物依次通过装有足量浓硫酸和碱石灰的装置完全吸收,则装有浓硫酸的装置质量增重________g,甲苯与C的物质的量之比为__________________。
【答案】酯键或酯基 C18H34O2 ![]() BD
BD ![]() + CH2=CH-CH3 →
+ CH2=CH-CH3 → ![]() CH3CH2CHO、CH2=CHOCH3 72 2:3
CH3CH2CHO、CH2=CHOCH3 72 2:3
【解析】
油脂A的分子式为C57H104O6,且反应生成C、D的物质的量之比为1: 3,则C为丙三醇,分子式为C3H8O3,根据一分子油脂水解生成三分子高级脂肪酸和一分子甘油可推出D的分子式为C18H34O2;石油裂解得到烯烃,E的分子式为C3H6O,则B也含有3个碳,为丙烯,E含有甲基且所有碳原子都是饱和碳原子,则为丙烯氧化得到,结构简式为![]() ,据此分析解答。
,据此分析解答。
油脂A的分子式为C57H104O6,且反应生成C、D的物质的量之比为1: 3,则C为丙三醇,分子式为C3H8O3,根据一分子油脂水解生成三分子高级脂肪酸和一分子甘油可推出D的分子式为C18H34O2;石油裂解得到烯烃,E的分子式为C3H6O,则B也含有3个碳,为丙烯,E含有甲基且所有碳原子都是饱和碳原子,则为丙烯氧化得到,结构简式为![]() 。
。
(1)G为![]() ,官能团的名称是酯基,D的分子式为C18H34O2,E的结构简式为
,官能团的名称是酯基,D的分子式为C18H34O2,E的结构简式为![]() ;
;
(2)A、苯甲酸的结构简式为![]() ,选项A错误;
,选项A错误;
B、苯甲酸苯环上有三种不同化学环境的氢,其一氯代物有3种,选项B正确;
C、苯甲酸中只有苯环能与氢气发生加成反应,则1个分子可与3个氢气分子发生加成反应,选项C错误;
D、苯甲酸与图中有机物C(丙三醇)反应可得到5种不同的酯类物质,将丙三醇中的三个羟基分别定位置为1、2、3,则一元酯化在1位、2位;二元酯化在1、2位,1、3位;三元酯化,共5种,选项D正确;
答案选BD;
(3)烃B为丙烯,与苯在一定条件下1:1反应生成F,分析F的1H核磁共振谱图,共有5个吸收峰,且峰面积之比为1:1:2:2:6,,则B为![]() ;B与苯反应生成F的化学方程式为
;B与苯反应生成F的化学方程式为![]() + CH2=CH-CH3 →
+ CH2=CH-CH3 → ![]() ;
;
(4)E为![]() ,其同分异构体①链状化合物;②氢谱上只有3组峰,则有三种不同环境下的氢原子,③分子中不含C=C—OH结构,符合条件的同分异构体有CH3CH2CHO、CH2=CHOCH3;
,其同分异构体①链状化合物;②氢谱上只有3组峰,则有三种不同环境下的氢原子,③分子中不含C=C—OH结构,符合条件的同分异构体有CH3CH2CHO、CH2=CHOCH3;
(5)甲苯分子式是C7H8,甘油分子式是C3H8O3,两者的相对分子质量都是92,所以无论两者比例如何,氢元素的质量分数 =![]() = 8.7%,甲苯与甘油的混合液体,其含碳量为60%,则含氧量为1-60%-8.7%=31.3%,取92g该混合液体完全燃烧,将产物依次通过装有足量浓硫酸和碱石灰的装置完全吸收,则装有浓硫酸的装置质量增重92g
= 8.7%,甲苯与甘油的混合液体,其含碳量为60%,则含氧量为1-60%-8.7%=31.3%,取92g该混合液体完全燃烧,将产物依次通过装有足量浓硫酸和碱石灰的装置完全吸收,则装有浓硫酸的装置质量增重92g ![]() =72g,92g该混合液体为1mol,设甲苯与甘油的物质的量分别为x、y,则有x+y=1,84x+36y=92
=72g,92g该混合液体为1mol,设甲苯与甘油的物质的量分别为x、y,则有x+y=1,84x+36y=92![]() 60%,联立解答得x=0.4mol,y=0.6mol,则甲苯与甘油的物质的量之比为2:3。
60%,联立解答得x=0.4mol,y=0.6mol,则甲苯与甘油的物质的量之比为2:3。

 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案