题目内容
(10分)目前世界上60%的镁是从海水中提取的,下图是某工厂从海水中提取镁的主要步骤。学生就这个课题展开了讨论。学生就这个课题提出了以下问题:
 (一)在海水提镁的过程中如何实现对镁离子的富集
(一)在海水提镁的过程中如何实现对镁离子的富集
有三个学生提出自己的观点。
 学生甲的观点:直接往海水中加入沉淀剂。
学生甲的观点:直接往海水中加入沉淀剂。
 学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。
学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。
 学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。
学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。
 通过分析比较你认为学生 的观点正确(填学生序号),简述理由:
通过分析比较你认为学生 的观点正确(填学生序号),简述理由:  。
。
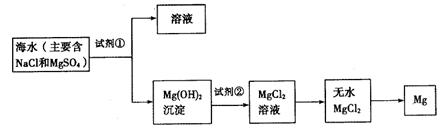


 (二)在海水提镁的过程中如何实现对镁离子的分离?
(二)在海水提镁的过程中如何实现对镁离子的分离?
 (1)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的足量试剂①是 (填化学式)。
(1)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的足量试剂①是 (填化学式)。
 (2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 (填标号字母)
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 (填标号字母)

 (3)加入的足量试剂②是 (填化学式)。
(3)加入的足量试剂②是 (填化学式)。
 (4)写出由无水MgCl2制取金属镁的化学方程式
(4)写出由无水MgCl2制取金属镁的化学方程式
 (一)在海水提镁的过程中如何实现对镁离子的富集
(一)在海水提镁的过程中如何实现对镁离子的富集
有三个学生提出自己的观点。
 学生甲的观点:直接往海水中加入沉淀剂。
学生甲的观点:直接往海水中加入沉淀剂。 学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。
学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。 学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。
学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。 通过分析比较你认为学生 的观点正确(填学生序号),简述理由:
通过分析比较你认为学生 的观点正确(填学生序号),简述理由:  。
。


 (二)在海水提镁的过程中如何实现对镁离子的分离?
(二)在海水提镁的过程中如何实现对镁离子的分离? (1)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的足量试剂①是 (填化学式)。
(1)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的足量试剂①是 (填化学式)。 (2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 (填标号字母)
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 (填标号字母)
| A.蒸馏 | B.过滤 | C.萃取 | D.分液 |
 (3)加入的足量试剂②是 (填化学式)。
(3)加入的足量试剂②是 (填化学式)。 (4)写出由无水MgCl2制取金属镁的化学方程式
(4)写出由无水MgCl2制取金属镁的化学方程式 (一)丙 镁离子富集浓度高;能源消耗小,成本低。
 (二)(1)Ca(OH)2(或CaO) (2)B
(二)(1)Ca(OH)2(或CaO) (2)B
 (3)HCl (4)MgCl2
(3)HCl (4)MgCl2 Mg+Cl2↑
Mg+Cl2↑
 (二)(1)Ca(OH)2(或CaO) (2)B
(二)(1)Ca(OH)2(或CaO) (2)B (3)HCl (4)MgCl2
(3)HCl (4)MgCl2 Mg+Cl2↑
Mg+Cl2↑略

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
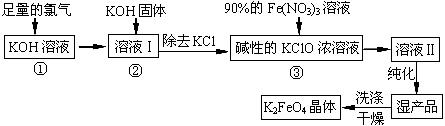

 时第一次通入Cl
时第一次通入Cl 表现 (填“氧化”或“还原”)性;
表现 (填“氧化”或“还原”)性;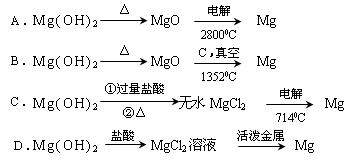
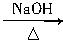 CH3CH2OH+HCl
CH3CH2OH+HCl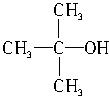 结构相似的醇不能被氧化成醛或羧酸。
结构相似的醇不能被氧化成醛或羧酸。
 的速度行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气。下列既可行又经济的制氢方法是 (填写编号)
的速度行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气。下列既可行又经济的制氢方法是 (填写编号) (4)今有两个氢气燃烧生成水的热化学方程式
(4)今有两个氢气燃烧生成水的热化学方程式
 O2(g)=CO2(g) △H=-283kJ/mol
O2(g)=CO2(g) △H=-283kJ/mol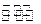 H2(g)+CO2(g)
H2(g)+CO2(g)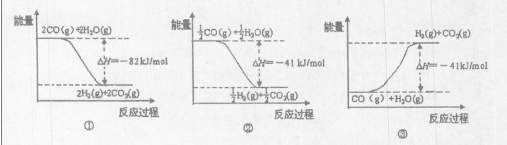
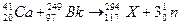 ,该变化不属于化学变化
,该变化不属于化学变化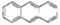 ),该分子中所有原子可以处于同一平面
),该分子中所有原子可以处于同一平面 Si+2CO↑制得粗硅
Si+2CO↑制得粗硅