��Ŀ����
1����ͼ����֪�����������ת��
��1��Aת��ΪB�������ⲽ��Ӧ��Ӧ������Լ��ǣ��ѧʽ��HCl��C��Һ�����ʵĻ�ѧʽKOH��
��2��д����Eת���F�Ļ�ѧ����ʽ4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��3��д������G��Һ�������ӵ����ӷ���ʽFe3++3SCN-=Fe��SCN��3����G��Һ�м���A���й����ӷ�Ӧ����ʽ��Fe+2Fe3+=3Fe2+��
��4����һƿ���ʱ��ϳ���B��Һ��ijѧ���������в������������ʣ�����б��ʣ�Ӧ��γ�ȥ���ʵ����ʣ�����Һ�м���������ԭ���ۣ�
���� ��ɫ����E�ڿ����б仯Ϊ���ɫ����F��˵��EΪFe��OH��2��FΪFe��OH��3��F�����ᷴӦ����GΪFeCl3������A���Ȼ�����Ӧ����B��B���C��Ӧ�õ�E��D����AΪFe��BΪFeCl2����Fe��Ԫ�ط�Ӧ�����������Ȼ�������D��Һ�������ữ����������Ӧ���ɰ�ɫ����HΪAgCl����Һ���ܲ���������ɫ��ӦΪ��ɫ��֤����Һ�к��м�Ԫ�أ���DΪKCl����CΪKOH���ݴ˽��н��
��� �⣺��ɫ����E�ڿ����б仯Ϊ���ɫ����F��˵��EΪFe��OH��2��FΪFe��OH��3��F�����ᷴӦ����GΪFeCl3������A���Ȼ�����Ӧ����B��B���C��Ӧ�õ�E��D����AΪFe��BΪFeCl2����Fe��Ԫ�ط�Ӧ�����������Ȼ�������D��Һ�������ữ����������Ӧ���ɰ�ɫ����HΪAgCl����Һ���ܲ���������ɫ��ӦΪ��ɫ��֤����Һ�к��м�Ԫ�أ���DΪKCl����CΪKOH��
��1��Aת����B��������Fe�����ᷴӦ�����Ȼ��������������������Լ��Ļ�ѧʽΪHCl��CΪ�������أ���ѧʽΪKOH��
�ʴ�Ϊ��HCl��KOH��
��2����Eת���F������������������Ϊ������������Ӧ�Ļ�ѧ����ʽΪ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��3����KSCN����G��FeCl3����Һ�����������ӣ���Ӧ�����ӷ���ʽΪ��Fe3++3SCN-=Fe��SCN��3��
��G��Һ�м���Fe���й����ӷ���ʽ�ǣ�Fe+2Fe3+=3Fe2+��
�ʴ�Ϊ��Fe3++3SCN-=Fe��SCN��3��Fe+2Fe3+=3Fe2+��
��4��FeCl2��Һ�����ʣ���Һ�л��������FeCl3��Ϊ�˲������µ����ʣ�������FeCl2��Һ�м������������ۣ���FeCl3�������ӻ�ԭ���������ӣ�
�ʴ�Ϊ������Һ�м���������ԭ���ۣ�
���� ����������ͼ�����ʽ������Fe��Cl��Ԫ�ص��ʼ��仯����֮����ת����ϵ�������а�ɫ����ת��Ϊ���ɫ��������ҺK��ɫ��ӦΪ��ɫ�Ƚ���ͻ�ƿڣ��Ѷ��еȣ�

| A�� | ��������NaOH���壬ƽ�������ƶ� | |
| B�� | ���£�ƽ�������ƶ���c��CH3COO-����С | |
| C�� | ��������CH3COONa���壬ƽ�������ƶ� | |
| D�� | ͨ������HCl���壬ƽ�������ƶ���c��H+����С |
| A�� | Na2O��Na2O2��ɫ��ͬ | |
| B�� | Na2O��Na2O2���Ǽ��������� | |
| C�� | Na2O��Na2O2��������Ư�ף�ɱ�������� | |
| D�� | �������ӵĸ����Ⱦ�Ϊ1��2 |
| A�� | 50mL 1.5mol/L��KCl��Һ | B�� | 50mL 1.5mol/L��KClO3��Һ | ||
| C�� | 100mL 1mol/L��MgCl��Һ | D�� | 450mL 0.5mol/��NaCl��Һ |

��1����֪��N2��g��+O2��g��=2NO��g����H=+a kJ•mol-1
N2��g��+3H2��g���T2NH3��g����H=-b kJ•mol-1
2H2��g��+O2��g��=2H2O��g����H=-c kJ•mol-1��a��b��c��Ϊ��ֵ��
����34g ��������������ȫ����һ�����������ˮ�������ų�������Ϊ$\frac{1}{2}$��2a-2b+3c��kJ��
��2���ϳ�NH3�ﵽƽ���ijʱ�̸ı���������A���ڴﵽ��ƽ��Ĺ���������Ӧ����ʼ������
A������ B����ѹ C������c��N2�� D������c��NH3��
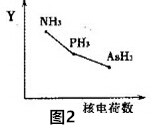
��3��ij����С���о����������������������£��ı���ʼ�����������ʵ����Ժϳ�NH3��Ӧ��Ӱ�죮ʵ������ͼ1��ʾ����ͼ��T��ʾ�¶ȣ�n��ʾ��ʼʱH2���ʵ�����
��ͼ����T2��T1�Ĺ�ϵ�ǣ�T2��T1�������������������=������ȷ��������
�ڱȽ���a��b��c����������ƽ��״̬�У���Ӧ��N2��ת����������c������ĸ����
���������ݻ�Ϊ1L��b���Ӧ��n=0.15mol�����ƽ��ʱH2��ת����Ϊ60%����ƽ��ʱN2�����ʵ���Ũ��Ϊ0.05 mol•L-1��
��4��һ���¶��£���2mol N2��4mol H2����1L�ĺ����ܱ������з�Ӧ����ò�ͬ��������ͬʱ����ںϳ�NH3��Ӧ��N2��ת���ʣ��õ��������±���
| ʱ�� N2��ת���� �¶� | 1Сʱ | 2Сʱ | 3Сʱ | 4Сʱ |
| T1 | 30% | 50% | 80% | 80% |
| T2 | 35% | 60% | a | b |
��5����ͼ2�л�����4����T1�¶���2mol N2��4mol H2��1L�����з�Ӧ��3Сʱ��ƽ��ǰ�������N2��NH3�����ʵ���Ũ����ʱ��ı仯����ͼ��
| A�� | 3��2 | B�� | 2��3 | C�� | 1��1 | D�� | 3��1 |
| A�� | Cl2 | B�� | NaClO | C�� | Na2O2 | D�� | NaOH |