题目内容
【题目】实验室里常用Na2O2与H2O反应快速制取少量的O2,下面装置用来制取O2并演示Na在O2中的燃烧实验。
(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气________(填“漏气”、“不漏气” 或“无法确定”)
(2)写出C装置中反应的化学方程式:_________
(3)若装置是不漏气的,打开止水夹a后,用上述装置进行实验。写出A中发生反应的化学方程式,并用双线桥标出化合价变化情况、电子转移的方向和数目及被氧化还原情况 _________
(4)B装置中盛放的试剂是__________,其作用是___________ D仪器名称是 _____
(5)Fe(OH)2 在潮湿空气中变成灰绿色、红褐色:_________

【答案】 漏气 2Na+O2 ![]() Na2O2
Na2O2 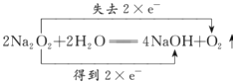 浓硫酸 干燥氧气 球形干燥管 4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3
浓硫酸 干燥氧气 球形干燥管 4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3
【解析】试题分析:(1)漏斗中的液体能全部流入试管说明试管中压强与外界相同;
(2) 钠与氧气在加热条件下生成过氧化钠;(3)A中过氧化钠与水反应生成氢氧化钠和氧气; (4)为防止A中的水蒸气与钠反应,B装置中盛放的试剂是浓硫酸,其作用是除去O2中的水蒸气;(5)Fe(OH)2 易被氧气氧化为氢氧化铁。
解析:(1) 关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。说明装置漏气,原因是漏斗中的液体能全部流入试管说明试管中压强与外界相同,若装置不漏气分液漏斗中的液体不能全部流入试管中;(2) 钠与氧气在加热条件下生成过氧化钠,反应方程式是2Na+O2 ![]() Na2O2;
Na2O2;
(3)A中过氧化钠与水反应生成氢氧化钠和氧气, A装置中反应的化学方程式并标出电子得失情况: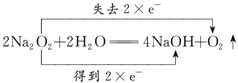 ;(3)为防止A中的水蒸气与钠反应,B装置中盛放的试剂是浓硫酸,其作用是干燥氧气,根据装置图D仪器名称是球形干燥管;(5)Fe(OH)2 易被氧气氧化为氢氧化铁,反应方程式是4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3。
;(3)为防止A中的水蒸气与钠反应,B装置中盛放的试剂是浓硫酸,其作用是干燥氧气,根据装置图D仪器名称是球形干燥管;(5)Fe(OH)2 易被氧气氧化为氢氧化铁,反应方程式是4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3。

【题目】T℃时,在2L恒容密闭容器中气态物质X、Y、Z的物质的量随时间变化的部分数据如表所示:
T/min | n(X)/mol | n(Y)/mol | n(Z)/mol |
0 | 0.80 | 1.00 | 0 |
1 | 0.70 | 0.80 | |
5 | 0.70 | ||
9 | 0.40 | ||
10 | 0.40 | 0.80 |
(1)写出该反应的化学方程式
(2)反应进行到10min,X的转化率为 , 0~5min内Y的平均反应速率为
(3)计算T℃时该反应的平衡常数K=
(4)T℃下向该密闭容器中通入一定量的X、Y、Z,反应到某时刻测得X、Y、Z的物质的量分别为1.00mol、0.50mol、1.60mol,则此时正逆反应速率大小:v正v逆(填“大于”、“等于”、“小于”)
(5)若在10min和t3、t5时刻分别改变该反应的某一反应条件,得到X、Z的物质的量及反应速率与时间的关系如图A、B所示: 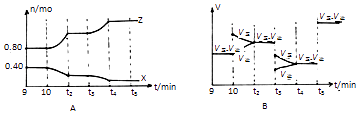
①10min时改变的反应条件是
②t3时刻改变的反应条件是t5时刻改变的反应条件是 , 理由是 .