题目内容
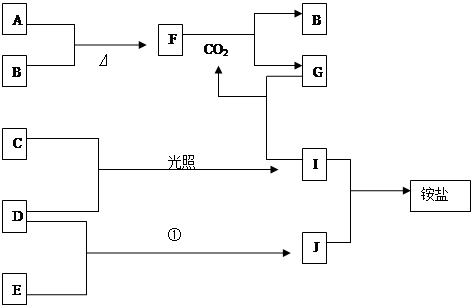
(16分)在通常状况下,A为固态单质。根据下图转化关系,回答:

(1)写出A、C、E的化学式:A__________,C__________,E__________。
(2)写出下列反应的化学方程式:
①E―→C :________________________________________________________;
②C―→D :________________________________________________________。
(3)B与E的浓溶液______发生反应(填“能”或“不能”),若能反应,则反应的化学方程式为____ ____,反应现象_________________________。

(1)写出A、C、E的化学式:A__________,C__________,E__________。
(2)写出下列反应的化学方程式:
①E―→C :________________________________________________________;
②C―→D :________________________________________________________。
(3)B与E的浓溶液______发生反应(填“能”或“不能”),若能反应,则反应的化学方程式为____ ____,反应现象_________________________。
(1)S SO2 H2SO4
(2)Cu + 2H2SO4 (浓) = CuSO4 + SO2 + 2H2O 2SO2 + O2 2SO3
2SO3
(3)能 H2S + H2SO4 =" S↓" + SO2↑ + 2H2O 产生淡黄色沉淀及无色有刺激性气味的气体
(2)Cu + 2H2SO4 (浓) = CuSO4 + SO2 + 2H2O 2SO2 + O2
 2SO3
2SO3(3)能 H2S + H2SO4 =" S↓" + SO2↑ + 2H2O 产生淡黄色沉淀及无色有刺激性气味的气体
固体单质A能和氧气反应,也能和氢气反应,说明是非金属单质。根据其氧化产物可用继续和氧气反应可判断,A是S,和氢气反应生成氯化氢,氯化物燃烧即生成SO2。硫和氧气反应是SO2,SO2和氧气反应生成三氧化硫,三氧化硫溶于水生成硫酸。浓硫酸在加热的条件下和铜发生氧化还原反应,生成硫酸铜、SO2和水。硫化氢中硫元素的化合价是—2价,处于最低价,具有还原性,而浓硫酸具有氧化性,二者发生氧化还原反应,生成硫单质和SO2以及水。

练习册系列答案
相关题目