题目内容
【题目】下列图示与对应的叙述相符的是
A.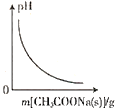 图表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
图表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.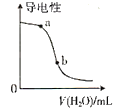 图表示向醋酸溶液中加水时其导电性变化,则CH3COOH溶液的pH:a点>b点
图表示向醋酸溶液中加水时其导电性变化,则CH3COOH溶液的pH:a点>b点
C.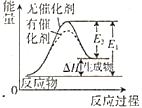 图表示催化剂能改变化学反应的焓变
图表示催化剂能改变化学反应的焓变
D. 图表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
图表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
【答案】D
【解析】
A.向CH3COOH溶液中逐渐加入CH3COONa固体,CH3COOH的电离平衡逆向移动,c(H+)减小,溶液pH增大,A错误;
B.向醋酸溶液中加水时其导电性减弱,CH3COOH溶液中c(H+)减小,pH:a点<b点,B错误;
C. 催化剂能降低反应的活化能,但不改变化学反应的焓变,C错误;
D. 在曲线的最低点,反应2NO2(g)N2O4(g)达平衡状态,在此点之后的所有点,都是该温度下的平衡点,由此可看出,升高温度,平衡逆向移动,则该反应的△H<0,D正确;
故选D。

【题目】氨气常用作合成氯氨类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2C1、NHCl2和NCl3),副产物少于其它水消毒剂。
回答下列问题:
(1)工业上可利用反应Cl2(g)+NH3(g)=NH2Cl(l)+HCl(g)制备一氯胺,已知部分化学键的键能如下表所示(假设不同物质中同种化学键的键能相同),则该反应的△H=___kJ/mol。
化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
键能(kJ/mol) | 391.3 | 243.0 | 191.2 | 431.8 |
一氯胺是重要的水消毒剂,其原因是由于一氯胺在中性、酸性环境中会发生完全水解,生成具有强烈杀菌消毒作用的物质,该水解反应的化学方程式为___。
(2)用Cl2和NH3反应制备二氯胺的方程式为2Cl2(g)+NH3(g)![]() NHCl2(g)+2HCl(g)。在恒温条件下,3molCl2和1molNH3发生反应,测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示:
NHCl2(g)+2HCl(g)。在恒温条件下,3molCl2和1molNH3发生反应,测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示:
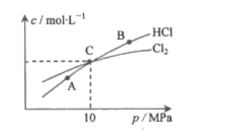
①A、B、C三点中Cl2转化率最高的是___点(填“A”“B”或“C")。
②计算C点时该反应的压强平衡常数Kp(C)=____(Kp是平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(3)我国研制出非贵金属镍钼基高效电催化剂,实现电解富尿素废水低能耗制H2(装置如图),总反应为:CO(NH2)2+H2O![]() 3H2↑+N2↑+CO2↑。
3H2↑+N2↑+CO2↑。

①A电极连接电源的___极(填"正”或“负”)。
②A电极的电极反应为___。