��Ŀ����
��0.2 mol��L-1NH4Cl��Һ��0.1 mol��L-1NaOH��Һ�������Ϻ���Һ�������������ʵ���Ũ�ȵĹ�ϵ��ȷ���ǣ� ��
A��c( )=c(Na+)=c(OH-)��c(NH3��H2O) )=c(Na+)=c(OH-)��c(NH3��H2O) |
B��c( )=c(Na+)��c(NH3��H2O)��c(OH-) )=c(Na+)��c(NH3��H2O)��c(OH-) |
C��c( )��c(Na+)��c(OH-)��c(NH3��H2O) )��c(Na+)��c(OH-)��c(NH3��H2O) |
D��c( )��c(Na+)��c(NH3��H2O)��c(OH-) )��c(Na+)��c(NH3��H2O)��c(OH-) |
D
��������Ŀ����������ѧ��Ӧ�����ȿ��ǻ�ѧ��Ӧ��ͨ����ѧ��Ӧ��������Ũ���ܱȽϳ������ؿ���ˮ��͵��룬��Ϊ������ʵ�����ε�ˮ��̶ȶ���С��������Ũ��Ӱ�첻����ͨ����ѧ��Ӧ��������Ũ�ȴ�С�Ƚϲ��������ٿ���ˮ���������ʵ��롣������NH4Cl��NaOH������Ӧ��NH4Cl+NaOH=NaCl+NH3��H2O����NH3��H2O��ͬʱ ��ʣ�࣬��������NH3��H2O�����
��ʣ�࣬��������NH3��H2O����� ˮ�⣬��c(NH3��H2O)=c(
ˮ�⣬��c(NH3��H2O)=c( )=c(Na+)="0.5" mol��L-1����ʱ���ǵ����ˮ�⣺NH3��H2O
)=c(Na+)="0.5" mol��L-1����ʱ���ǵ����ˮ�⣺NH3��H2O
 +OH-��,
+OH-��,  +H2O
+H2O NH3��H2O+H+�ڡ��ٷ���ʹ��Һc(
NH3��H2O+H+�ڡ��ٷ���ʹ��Һc( )���ڷ�Ӧʹ��Һc(
)���ڷ�Ӧʹ��Һc( )��С����Һc(
)��С����Һc( )�������Ǽ�С��ȡ����������Ӧ��һ��Ϊ��Ҫ�����ݾ�������֪���ε�ˮ���������ʵĵ��룬�Ե���Ϊ�������c(
)�������Ǽ�С��ȡ����������Ӧ��һ��Ϊ��Ҫ�����ݾ�������֪���ε�ˮ���������ʵĵ��룬�Ե���Ϊ�������c( )������c(Na+)��ͬ��c(NH3��H2O)Ӧ���٣�С��c(Na+)����Һ��c(OH-)����NH3��H2O���룬���������c(OH-)Ũ�Ⱥ�С������Ũ��˳��Ϊc(
)������c(Na+)��ͬ��c(NH3��H2O)Ӧ���٣�С��c(Na+)����Һ��c(OH-)����NH3��H2O���룬���������c(OH-)Ũ�Ⱥ�С������Ũ��˳��Ϊc( )��c(Na+)��c(NH3��H2O)��c(OH-)��
)��c(Na+)��c(NH3��H2O)��c(OH-)��
 ��ʣ�࣬��������NH3��H2O�����
��ʣ�࣬��������NH3��H2O����� ˮ�⣬��c(NH3��H2O)=c(
ˮ�⣬��c(NH3��H2O)=c( )=c(Na+)="0.5" mol��L-1����ʱ���ǵ����ˮ�⣺NH3��H2O
)=c(Na+)="0.5" mol��L-1����ʱ���ǵ����ˮ�⣺NH3��H2O
 +OH-��,
+OH-��,  +H2O
+H2O NH3��H2O+H+�ڡ��ٷ���ʹ��Һc(
NH3��H2O+H+�ڡ��ٷ���ʹ��Һc( )���ڷ�Ӧʹ��Һc(
)���ڷ�Ӧʹ��Һc( )��С����Һc(
)��С����Һc( )�������Ǽ�С��ȡ����������Ӧ��һ��Ϊ��Ҫ�����ݾ�������֪���ε�ˮ���������ʵĵ��룬�Ե���Ϊ�������c(
)�������Ǽ�С��ȡ����������Ӧ��һ��Ϊ��Ҫ�����ݾ�������֪���ε�ˮ���������ʵĵ��룬�Ե���Ϊ�������c( )������c(Na+)��ͬ��c(NH3��H2O)Ӧ���٣�С��c(Na+)����Һ��c(OH-)����NH3��H2O���룬���������c(OH-)Ũ�Ⱥ�С������Ũ��˳��Ϊc(
)������c(Na+)��ͬ��c(NH3��H2O)Ӧ���٣�С��c(Na+)����Һ��c(OH-)����NH3��H2O���룬���������c(OH-)Ũ�Ⱥ�С������Ũ��˳��Ϊc( )��c(Na+)��c(NH3��H2O)��c(OH-)��
)��c(Na+)��c(NH3��H2O)��c(OH-)��
��ϰ��ϵ�д�
�����Ŀ
 Mg2++2OH- ��
Mg2++2OH- �� +H2O
+H2O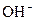 ��
��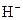 ��
��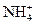 ��
��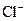 �������ӣ���Ũ�ȴ�С�����¹�ϵ�����п��ܵ��ǣ�����
�������ӣ���Ũ�ȴ�С�����¹�ϵ�����п��ܵ��ǣ�����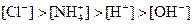
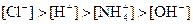
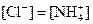 ��
��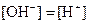
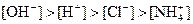
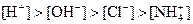
 ��С
��С