题目内容
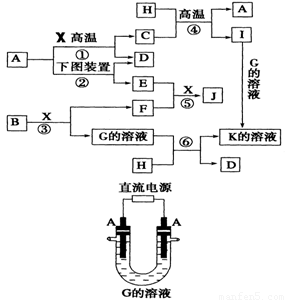
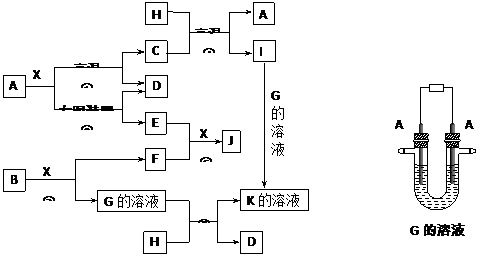
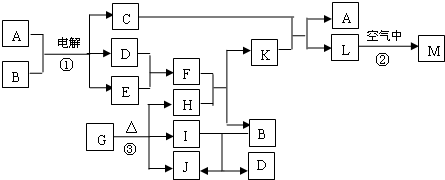
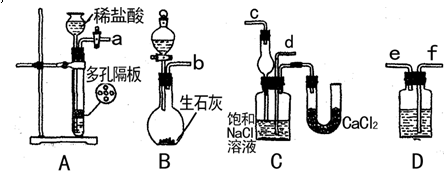
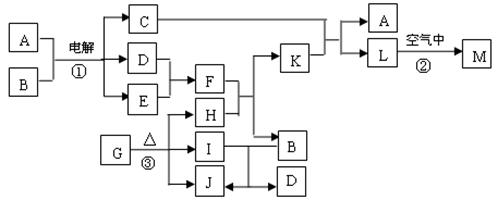
下图表示各物质之间的转化关系。已知:A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液。
 |
请按要求填空:
⑴写出B的电子式: 。
⑵写出用A作电极电解G溶液,在电极上生成E的反应式: ,反应⑤的现象是 。
⑶反应①的化学方程式是 ,反应④在生产中有重要应用,被称为 反应。
⑷反应⑥的离子方程式是 。
⑴Na+[![]() ]2-Na+ (2分)
]2-Na+ (2分)
⑵Fe+2OH――2e-=Fe(OH)2 (2分)白色物质迅速转变为灰绿色最终变为红褐色(2分)
⑶3Fe+4H2O![]() Fe3O4+4H2 (2分) 铝热(1分)
Fe3O4+4H2 (2分) 铝热(1分)
⑷2Al+2OH-+2H2O=2AlO2-+3H2↑(2分)
解析:
本题以框图的形式考查元素化合物之间的转化关系及电化学知识;X常温下为无色液体,可确定为H2O,B为淡黄色固体,且可与水反应生成气体单质,且B为Na2O2,G为氢氧化钠溶液,F为O2;A既能与水在高温下反应生成单质D,又可做电极电解氢氧化钠溶液得到D,且E在氧气和水的作用下得到J,J溶于酸为黄色溶液,则A为铁,C为四氧化三铁,D为氢气,D为氢氧化亚铁,J为氢氧化铁;H既能与氢氧化钠溶液反应,又能与四氧化三铁反应,故为金属铝,由此可知I 为氧化铝,K为偏铝酸钠溶液。(1)过氧化钠为离子化合物,电子式为Na+[![]() ]2-Na+;(2)铁为活性电极,在阳极首先放电,生成E的电极反应式为Fe+2OH――2e-=Fe(OH)2,氢氧化亚铁不稳定,在空气中迅速由白色变成灰绿色最终变为红褐色;(3)铝与金属氧化物之间的反应被称为铝热反应;(4)铝在氢氧化钠溶液中反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑。
]2-Na+;(2)铁为活性电极,在阳极首先放电,生成E的电极反应式为Fe+2OH――2e-=Fe(OH)2,氢氧化亚铁不稳定,在空气中迅速由白色变成灰绿色最终变为红褐色;(3)铝与金属氧化物之间的反应被称为铝热反应;(4)铝在氢氧化钠溶液中反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑。

 .
.