题目内容
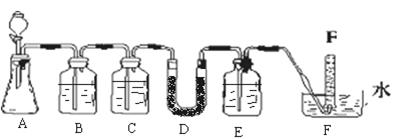
Na2S2O3·5H2O在化学定量分析中常用作基准物质,实验室制备原理为:2Na2S+Na2CO3+4SO2 3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
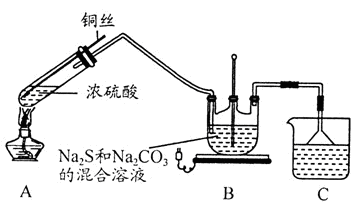
(1)A中发生的化学反应方程式为 。
(2)C中所盛试剂可能是 ;若要停止A中的化学反应,除取下酒精灯停止加热外,还可以采取的操作是 。
(3)学生乙在加热A后,发现液面下的铜丝变黑。对黑色生成物该学生提出如下假设:
①可能是CuO ②可能是Cu2O ③可能是CuS
学生丙提出假设②一定不成立,依据是 ;该生用如下实验进一步验证黑色物质的组成:
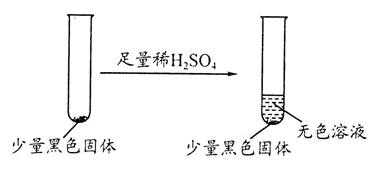
基于上述假设分析,黑色物质的组成为 (填化学式)。
(4)实验室用Na2S2O3标液测量废水Ba2+的浓度,过程如下:
(已知:2 S2O32一+I2=S4O62—+2 I-)

①写出BaCrO4沉淀与过量HI、HCl溶液反应的离子方程式 ;
②以淀粉为指示剂,则到达滴定终点的现象是 ;
③若标液Na2S2O3的浓度0.0030mol·L-1,消耗该Na2S2O3溶液体积如图,则废水Ba2+的浓度为 。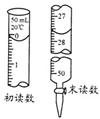
 3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
(1)A中发生的化学反应方程式为 。
(2)C中所盛试剂可能是 ;若要停止A中的化学反应,除取下酒精灯停止加热外,还可以采取的操作是 。
(3)学生乙在加热A后,发现液面下的铜丝变黑。对黑色生成物该学生提出如下假设:
①可能是CuO ②可能是Cu2O ③可能是CuS
学生丙提出假设②一定不成立,依据是 ;该生用如下实验进一步验证黑色物质的组成:

基于上述假设分析,黑色物质的组成为 (填化学式)。
(4)实验室用Na2S2O3标液测量废水Ba2+的浓度,过程如下:
(已知:2 S2O32一+I2=S4O62—+2 I-)

①写出BaCrO4沉淀与过量HI、HCl溶液反应的离子方程式 ;
②以淀粉为指示剂,则到达滴定终点的现象是 ;
③若标液Na2S2O3的浓度0.0030mol·L-1,消耗该Na2S2O3溶液体积如图,则废水Ba2+的浓度为 。

(1)Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O(2)氢氧化钠溶液 可将铜丝抽离液面已停止反应
(3)Cu2O为砖红色
(4)2BaCrO4+6I-+16H+=3I2+2Cr3++2Ba2++8H2O 滴入最后一滴溶液,锥形瓶内溶液有蓝色变为无色,维持30s不变, 0.0011mol/L
试题分析:(1)金属铜和浓硫酸反应生成二氧化硫气体,根据质量守恒定律不难写出相关化学方程式。(2)
吸收未反应的二氧化硫气体和生成的二氧化碳气体,采用的尾气处理溶液为氢氧化钠溶液。把铜丝抽
离液面反应就可以停止。(3)氧化亚铜颜色为红色的;黑色物质不溶于硫酸,所以该黑色物质不可能是
氧化铜,应该是硫化铜;(4)?根据反应物和生成物不难写出相关离子方程式;当滴入最后一滴溶液,
锥形瓶内溶液由蓝色变成无色,且保持30s不变;消耗该Na2S2O3溶液体积,27.80ml-0.30ml=27.50ml,
关系式:Ba2+ - BaCrO4 -
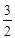 I2 -3 S2O32一;n(Ba2+)=
I2 -3 S2O32一;n(Ba2+)=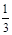 ×27.50×10-3L×0.0030mol·L-1=2.75×10-5mol,Ba2+的浓度为:
×27.50×10-3L×0.0030mol·L-1=2.75×10-5mol,Ba2+的浓度为: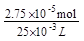 =1.1×10-3mol·L-1。
=1.1×10-3mol·L-1。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
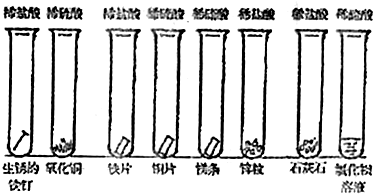
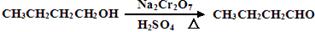 。反应物和产物的相关数据列表如下:
。反应物和产物的相关数据列表如下: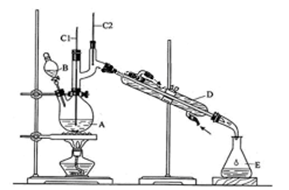
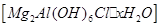 是一种新型离子交换材料,其在高温下完全分解为
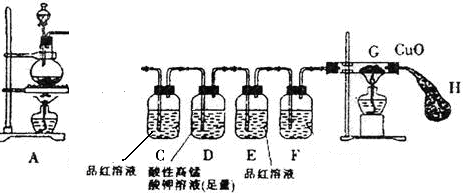
是一种新型离子交换材料,其在高温下完全分解为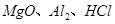 和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。
和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。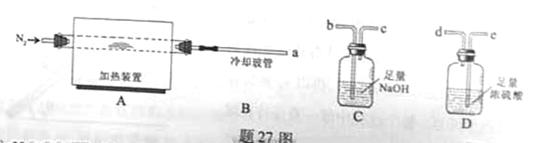
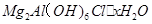 热分解的化学方程式为 。
热分解的化学方程式为 。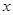 ,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。
,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。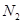 排尽装置中的空气,称取C、D的初始质量后,再持续通入
排尽装置中的空气,称取C、D的初始质量后,再持续通入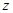 ,除测定D的增重外,至少还需测定 .
,除测定D的增重外,至少还需测定 .