��Ŀ����
����Ŀ��һ������![]() �ں�ѹ�ܱ������з�����Ӧ��
�ں�ѹ�ܱ������з�����Ӧ��![]() ��ƽ��ʱ����ϵ�и���������������¶ȵĹ�ϵ��ͼ��ʾ��
��ƽ��ʱ����ϵ�и���������������¶ȵĹ�ϵ��ͼ��ʾ��

(1).��֪���顢̼��������ȼ���ȷֱ�Ϊ![]() ��
��![]() ��
��![]() ����÷�Ӧ�ķ�Ӧ��
����÷�Ӧ�ķ�Ӧ��![]() __________��
__________��
(2).������˵����Ӧһ���ﵽƽ��״̬����_______��
![]() ��
��![]() ������������
������������
![]() ��������ƽ����Է�����������
��������ƽ����Է�����������
![]() ���������ܶȲ���
���������ܶȲ���
![]() ������ѹǿ���ٱ仯
������ѹǿ���ٱ仯
![]() ̼���������ٸı�
̼���������ٸı�
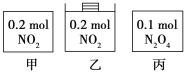
(3).![]() ʱ������ƽ����ϵ�г���������壬��ʱ��Ӧ����____
ʱ������ƽ����ϵ�г���������壬��ʱ��Ӧ����____![]() ���������������С������������
���������������������������![]() ����
����![]() _____
_____![]() ����
����![]() ������
������![]() ������
������![]() ��
��![]() ��
��
(4).![]() ʱ������ƽ����ϵ�г���������
ʱ������ƽ����ϵ�г���������![]() ��
��![]() ����ƽ��_____�ƶ�����������_______��
����ƽ��_____�ƶ�����������_______��
(5).![]() ʱ����Ӧ��ƽ���
ʱ����Ӧ��ƽ���![]() ��ת����Ϊ____________��
��ת����Ϊ____________��
���𰸡�![]()
![]() ��С
��С ![]() ���ƶ�
���ƶ� ![]() ��
��![]() ��Ũ�Ȳ���
��Ũ�Ȳ��� ![]()
��������
���⿼�鷴Ӧ�ȵļ��㣬��ѧƽ���ƶ�����ѧƽ��״̬���жϣ��Ѷ��еȡ�
(1).��֪���顢̼��������ȼ���ȷֱ�Ϊ![]() ��
��![]() ��
��![]() ������
������
![]() ��
��![]()
![]() ��
��
���ݸ�˹����![]() �õ�Ŀ�귽��ʽ��
�õ�Ŀ�귽��ʽ��
(2).![]() �����ݻ�ѧƽ���ֱ�Ӻͼ���ж������жϣ�
�����ݻ�ѧƽ���ֱ�Ӻͼ���ж������жϣ�
(3).���º�ѹ��������壬�൱�ڷ�Ӧ��Ũ�ȼ�С�����ʼ�С��ƽ�������ƶ���
(4).![]() ʱ������ƽ����ϵ�г���������
ʱ������ƽ����ϵ�г���������![]() ��
��![]() ����ƽ�ⲻ�ƶ�����Ϊ
����ƽ�ⲻ�ƶ�����Ϊ![]() ��
��![]() ��Ũ�Ȳ��䣻
��Ũ�Ȳ��䣻
(5).![]() ʱ���������������Ϊ�ٷ�֮��ʮ��������ʽ���㷴Ӧ��ƽ���
ʱ���������������Ϊ�ٷ�֮��ʮ��������ʽ���㷴Ӧ��ƽ���![]() ��ת���ʣ�
��ת���ʣ�
![]() ��֪���顢̼��������ȼ���ȷֱ�Ϊ
��֪���顢̼��������ȼ���ȷֱ�Ϊ![]() ��
��![]() ��
��![]() ������
������
![]() ��
��![]()
![]() ��
��
���ݸ�˹����![]() �ã�
�ã�![]()
![]() ����÷�Ӧ�ķ�Ӧ��
����÷�Ӧ�ķ�Ӧ��![]() ��
��
�ʴ�Ϊ��![]() ��
��
![]() ��
��![]() �����������ȣ�����˵����Ӧһ���ﵽƽ��״̬����a����
�����������ȣ�����˵����Ӧһ���ﵽƽ��״̬����a����
![]() ����̼Ϊ���壬�ҷ�Ӧǰ���������������ȣ���˻�������ƽ����Է����������䣬��˵����Ӧһ���ﵽƽ��״̬����b��ȷ��
����̼Ϊ���壬�ҷ�Ӧǰ���������������ȣ���˻�������ƽ����Է����������䣬��˵����Ӧһ���ﵽƽ��״̬����b��ȷ��
![]() ����̼Ϊ���壬���Ի��������ܶȲ��䣬��˵����Ӧһ���ﵽƽ��״̬����c��ȷ��
����̼Ϊ���壬���Ի��������ܶȲ��䣬��˵����Ӧһ���ﵽƽ��״̬����c��ȷ��
![]() ��Ϊ��Ӧ�ں�ѹ�����½��У�����������ѹǿ���ٱ仯������˵����Ӧһ���ﵽƽ��״̬����d����
��Ϊ��Ӧ�ں�ѹ�����½��У�����������ѹǿ���ٱ仯������˵����Ӧһ���ﵽƽ��״̬����d����
![]() ̼���������ٸı䣬��˵����Ӧһ���ﵽƽ��״̬����e��ȷ��
̼���������ٸı䣬��˵����Ӧһ���ﵽƽ��״̬����e��ȷ��
�ʴ�Ϊ��bce��
![]() ʱ����Ϊ��Ӧ�ں�ѹ�����½��У�����ƽ����ϵ�г���������壬�������Ӧ��Ũ�ȼ�С�����Է�Ӧ���ʱ�С��ƽ�������ƶ�����
ʱ����Ϊ��Ӧ�ں�ѹ�����½��У�����ƽ����ϵ�г���������壬�������Ӧ��Ũ�ȼ�С�����Է�Ӧ���ʱ�С��ƽ�������ƶ�����![]() ��
��
�ʴ�Ϊ����С��![]() ��
��
![]() ʱ������ƽ����ϵ�г���������
ʱ������ƽ����ϵ�г���������![]() ��
��![]() ����ƽ�ⲻ�ƶ�����Ϊ
����ƽ�ⲻ�ƶ�����Ϊ![]() ��
��![]() ��Ũ�Ȳ��䣻
��Ũ�Ȳ��䣻
�ʴ�Ϊ�����ƶ���![]() ��
��![]() ��Ũ�Ȳ��䣻
��Ũ�Ȳ��䣻
![]()
![]()
��ʼ(mol)
ת��(mol) x 2x
ƽ��(mol) ![]() 2x
2x
��![]() �����
�����![]() ������
������![]() ʱ����Ӧ��ƽ���
ʱ����Ӧ��ƽ���![]() ��ת����Ϊ
��ת����Ϊ![]() ��
��
�ʴ�Ϊ��![]() ��
��

 �ƸԹھ��ο���ϵ�д�
�ƸԹھ��ο���ϵ�д� ������ҵ��ͬ����ϰ��ϵ�д�
������ҵ��ͬ����ϰ��ϵ�д�