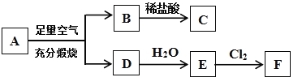
题目内容
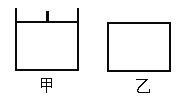
【题目】已知甲为恒压容器、乙为恒容容器。相同条件下充入等物质的量NO2气体,且起始时体积相同。发生反应:2NO2(g)![]() N2O4(g) △H<0。一段时间后均达到平衡状态。下列说法中正确的是
N2O4(g) △H<0。一段时间后均达到平衡状态。下列说法中正确的是
A. 平衡时NO2体积分数:甲<乙
B. 达到平衡所需时间,甲与乙相等
C. 该反应的平衡常数表达式K=c(N2O4)/c(NO2)
D. 若两容器内气体的压强保持不变,均说明反应已达到平衡状态
【答案】A
【解析】A、反应起始时,二氧化氮的浓度相同、温度相同、压强相同,反应速率相同,随反应进行,容器乙中压强降低,容器甲体积可变,压强不变,故反应达到平衡时,两容器内的压强关系是p(甲)>p(乙),甲中平衡正向进行,平衡时NO2体积分数减小,甲<乙,故A正确;
B、容器乙体积不变,随反应进行,反应混合气体的物质的量减小,容器乙中压强降低,容器甲体积可变,压强不变,压强越大,反应速率越快,达到平衡所需时间甲短,故B错误;
C、平衡常数K=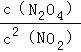 ,故C错误;
,故C错误;
D、容器乙体积不变,随反应进行,反应混合气体的物质的量减小,容器乙中压强降低,容器甲体积可变,压强不变,故反应达到平衡时,两容器内的压强关系是p(甲)<p(乙),甲容器始终不变,故D错误;
故选A.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目