题目内容
【题目】某课外探究活动小组使用常用仪器,运用实验室制备氢气的原理,巧妙设计了如图所示的简单实验装置。
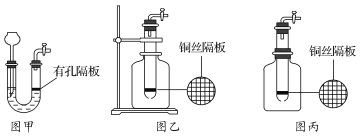
甲同学设计了如图甲所示装置:
①检查该装置气密性的方法是_________
②实验时若液面不能与锌粒接触,又无酸液可加,且该装置已固定,则使反应发生的操作是_____
(2)乙同学把试管底部钻一小洞,并和广口瓶组装成如图乙所示具有启普发生器功能的装置,若该装置中的隔板是用铜丝制成的,隔板上放锌粒,酸使用H2SO4,写出反应的离子方程式:_____
(3)丙同学设计了如图丙所示装置,即用橡皮塞代替铁架台来固定试管,则丙同学的做法________(填“可行”或“不可行”),理由是______________
【答案】关闭活塞,从长颈漏斗向U形管中加水,若长颈漏斗中形成一段稳定的水柱,说明装置气密性良好 从长颈漏斗加入少量蒸馏水使溶液与锌粒接触 Zn+2H+=Zn2++H2↑ 不可行 广口瓶被橡皮塞密封后,瓶内的气压会随液体的加入而增大,使试管中的液体不能在关闭阀门时排入广口瓶中,因而不能使反应随时停止,甚至会由于容器中气压过高而发生危险
【解析】
(1)①设法使装置内外形成气压差是气密性检查的常用手段,据此分析;
②根据实验时若液面刚好不与锌粒接触,而又无酸液,且该装置已固定,可以加蒸馏水使酸和锌接触分析;
(2)锌和稀硫酸反应生成硫酸锌与氢气;
(3)根据能否造成安全事故分析判断,如果容器内压强过大,会造成安全事故。
(1)①气密性检验的方法是:关闭活塞,从长颈漏斗向U形管中加水,若长颈漏斗中形成一段稳定的水柱,说明装置气密性良好;
②实验时若液面刚好不与锌粒接触,而又无酸液可加,且该装置已固定,可以加蒸馏水使酸和锌接触,即从长颈漏斗加入少量蒸馏水使溶液与锌粒接触;
(2)锌粒会与稀硫酸反应,其离子方程式为:Zn+2H+=Zn2++H2↑;
(3)由于广口瓶被橡皮塞密封后,瓶内的气压会随液体的加入而增大,使试管中的液体不能在关闭阀门时排入广口瓶中,因而不能使反应随时停止,甚至会由于容器中气压过高而发生危险,所以该做法不可行,故答案为:不可行;广口瓶被橡皮塞密封后,瓶内的气压会随液体的加入而增大,使试管中的液体不能在关闭阀门时排入广口瓶中,因而不能使反应随时停止,甚至会由于容器中气压过高而发生危险。

【题目】烃分子中若含有双键,叁键或环,其碳原子所结合的氢原子则少于同碳原子数对应烷烃所含的氢原子数,亦具有一定的不饱和度(用W表示)。下表列出几种烃的不饱和度:
有机物 | 乙烯 | 乙炔 | 环己烷 | 苯 |
W | 1 | 2 | 1 | 4 |
据此下列说法不正确的是
A. 1molW=3的不饱和链烃再结合6molH即达到饱和
B. ![]() 的W等于6
的W等于6
C. CH3CH2CH=CH2与环丁烷的不饱和度相同
D. C4H8的不饱和度与C3H6、C2H4的不饱和度不相同