题目内容
5.0.5molNa2SO4( )| A. | 含3.01×1023个SO42- | B. | 标准状况下,体积约为11.2L | ||
| C. | 含0.5molNa+ | D. | 含1mol氧原子 |
分析 A.硫酸根物质的量等于硫酸钠物质的量,根据N=nNA计算硫酸根数目;
B.硫酸钠是固体,不是气体;
C.钠离子物质的量为硫酸钠的2倍;
D.氧原子物质的量为硫酸钠的4倍.
解答 解:A.0.5molNa2SO4中含SO42-数目为0.5mol×6.02×1023mol-1=3.01×1023,故A正确;
B.硫酸钠是固体,不是气体,不能用气体摩尔体积计算其体积,故B错误;
C.0.5molNa2SO4中含Na+为0.5mol×2=1mol,故C错误;
D.氧原子物质的量为硫酸钠的4倍,故0.5molNa2SO4中含氧原子为0.5mol×4=2mol,故D错误,
故选A.
点评 本题考查物质的量有关计算,比较基础,侧重对基础知识的巩固,注意气体摩尔体积的使用条件与对象.

练习册系列答案
相关题目
16.一定温度下,可逆反应A(g)+3B(g)?2C(g)达到限度的标志是( )
| A. | C的生成速率与A的消耗速率相等 | |
| B. | 单位时间生成nmolA,同时生成3nmolB | |
| C. | A、B、C的浓度不再变化 | |
| D. | A、B、C的分子数之比为1:3:2 |
13.下列关于吸热反应和放热反应的说法正确的是( )
| A. | 需加热才能发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温条件一定能发生 | |
| C. | 反应物和生成物分别具有的总能量决定了反应是放热反应还是吸热反应 | |
| D. | 当△H<0时表明反应为吸热反应 |
20.下列物质分离方法不正确的是( )
| A. | 用过滤的方法除去食盐水中的泥沙 | |
| B. | 用酒精萃取碘水中的碘 | |
| C. | 用分液的方法分离汽油和氯化钠溶液 | |
| D. | 用蒸馏的方法将自来水制成蒸馏水 |
10.海水淡化是应对水短缺的重要手段,所谓海水淡化是指除去海水中的盐分以获得淡水的工艺过程.下列方法中可以用来进行海水淡化的是( )
| A. | 过滤法 | B. | 蒸馏法 | C. | 分液法 | D. | 萃取法 |
17.25℃时,将稀氨水逐滴滴加到稀硫酸中,当溶液的pH=7时,下列关系正确的是( )
| A. | c(NH4+)=c(SO42-) | B. | c(NH4+)>c(SO42-) | ||
| C. | c(NH4+)<c(SO42-) | D. | c(NH4+)+c(SO42-)=c(H+)+c(NH4+) |
14.下列方程式书写正确的是( )
| A. | NaHCO3的电离方程式:NaHCO3═Na++H++CO32- | |
| B. | 往AlCl3溶液中滴加NaHCO3溶液:Al3++3HCO3-═Al(OH)3↓+3CO2↑ | |
| C. | 往AgI悬浊液中滴加Na2S饱和溶液:2Ag++S2-═Ag2S↓ | |
| D. | Cu(NO3)2溶液电解的离子方程式:2Cu2++2H2O═2Cu+O2↑+4H+ |
18.下列各组物质中,互为同分异构体的是( )
| A. | 2-甲基丙烷 正丁烷 | B. | 氧气 臭氧 | ||
| C. | 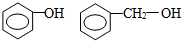 | D. | 金刚石 石墨 |