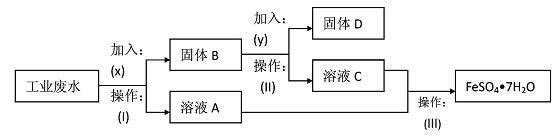
题目内容
【题目】高炉炼铁中常见的反应为:Fe2O3(s)+3CO(g) ![]() 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H
(1)某实验小组在实验室模拟上述反应。一定温度下,在2L盛有Fe2O3粉末的恒容密闭容器中通入0.1molCO,5min时生成2.24gFe。5min内有CO表示的平均反应速率是mol·L-1min-1;5min时CO2的体积分数为;若将此时反应体系中的混合气体通入100mL0.9mol/L的NaOH溶液中,充分反应后所得溶液中离子浓度由大到小的顺序是 。
(2)上述反应的平衡常数表达式为:K=;下列能说明该反应已经达到平衡状态的是(填序号)。
a.容器内固体质量保持不变
b.容器中气体压强保持不变
c.c(CO)=c(CO2)
d.v正(CO)=v逆(CO2)
(3)已知上述反应的平衡常数K与温度T(单位:K)之间的关系如图所示,其中直线的斜率为- ![]() (气体常数R=8.3×10-3kJ·mol-1·K-1)。
(气体常数R=8.3×10-3kJ·mol-1·K-1)。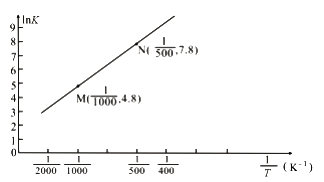
①根据图像可知,该反应的平衡常数随温度升高而(填“增大”、“减小”或“不变”)
②该反应的△H=kJ·mol-1。
(4)结合上述有关信息,写出两条提高CO转化率的措施、。
【答案】
(1)0.006;60%;c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
(2)c3(CO2)/c3(CO);ad
(3)减小;-24.9
(4)降低CO2的浓度;适当降低温度
【解析】高炉炼铁中常见的反应为:Fe2O3(s)+3CO(g) ![]() 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H
(1)n(Fe)=2.24g÷56g/mol=0.04mol,由反应可知消耗CO为0.04mol× ![]() =0.06mol,则10min内CO的平均反应速率为v=
=0.06mol,则10min内CO的平均反应速率为v= ![]() =0.006 mol/(L·min);将混合气体通入100mL0.9mol/L的NaOH溶液中,完全反应后可得0.03molNaHCO3和0.03molNa2CO3的混合溶液,因水解溶液显碱性,且CO32-的水解程度大于HCO3- , 所得溶液中离子浓度由大到小的顺序是 c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) ;
=0.006 mol/(L·min);将混合气体通入100mL0.9mol/L的NaOH溶液中,完全反应后可得0.03molNaHCO3和0.03molNa2CO3的混合溶液,因水解溶液显碱性,且CO32-的水解程度大于HCO3- , 所得溶液中离子浓度由大到小的顺序是 c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) ;
(2)由Fe2O3(s)+3CO(g) ![]() 2Fe(s)+3CO2(g),纯固体不能代入K的表达式中,则该反应的化学平衡常数表达式为K=
2Fe(s)+3CO2(g),纯固体不能代入K的表达式中,则该反应的化学平衡常数表达式为K= ![]() ;a.容器内固体质量保持不变,能说明是平衡状态,故a正确;b.因容器中气体的总物质的量不变,压强保持不变无法说明是平衡状态,故b错误;c.c(CO)=c(CO2) 无法说明是平衡状态,故c错误;d.当v正(CO)=v逆(CO2) 时能说明是平衡状态,故d正确;故答案为ad;
;a.容器内固体质量保持不变,能说明是平衡状态,故a正确;b.因容器中气体的总物质的量不变,压强保持不变无法说明是平衡状态,故b错误;c.c(CO)=c(CO2) 无法说明是平衡状态,故c错误;d.当v正(CO)=v逆(CO2) 时能说明是平衡状态,故d正确;故答案为ad;
(3)①根据图像可知,lnK随 ![]() 增大而增大,而温度越高,
增大而增大,而温度越高, ![]() 越小,则该反应的平衡常数随温度升高而减小;
越小,则该反应的平衡常数随温度升高而减小;
②设直线与纵轴交点的纵坐标是b,则有lnK=- ![]() +b,将M、N两点的坐标数值代入求得b=1.8,则有4.8= -
+b,将M、N两点的坐标数值代入求得b=1.8,则有4.8= - ![]() +1.8,解得△H=-24.9kJ·mol-1;
+1.8,解得△H=-24.9kJ·mol-1;
(4)此反应正方向为放热反应,可以通过 降低CO2的浓度或适当降低温度,使平衡正向移动,达到提高CO转化率的目的。
(1)根据化学反应速率的定义计算;根据二氧化碳与氢氧化钠的反应判断生成产物的主要成分,然后比较溶液中离子浓度的大小关系即可;
(2)根据化学平衡常数的定义进行书写表达式;根据可逆反应达到平衡状态的特点判断是否达到平衡状态;
(3)根据化学平衡常数与温度的关系进行判断;根据图中的数据计算反应热;
(4)根据外界条件对化学平衡的影响判断改变的条件。

 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】I、硬质玻璃管是化学实验中经常使用的一种仪器,分析下列实验并回答:
如图1所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c 三个棉球变化如下表(认为所产生的气体与棉球上的试剂均得到充分的反应)。则浓硫酸在该反应中表现的性质_________________;
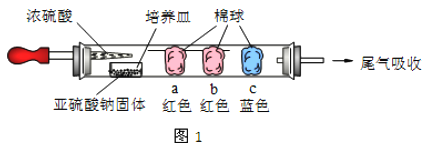
棉球 | 棉球上滴加试剂 | 实验现象 | 解释或结论 |
a | ___________ | 棉球变白,微热后又恢复红色 | 该气体具有______性。 |
b | 含酚酞的NaOH 溶液 | 棉球变为白色 | 离子方程式_________ |
c | __________ | 棉球变为白色 | 化学方程式___________,该气体具有_______性。 |
II.通常情况下,向硫酸亚铁溶液中滴加氢氧化钠溶液时,生成的白色絮状沉淀会迅速变为_____色,最终变为____色写出上述白色絮状沉淀变化过程的化学方程式_______;
用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一: 用不含O2的蒸馏水配制的NaOH 溶液与硫酸亚铁反应制备。
(1)除去蒸馏水中溶解的O2常采用_________的方法。
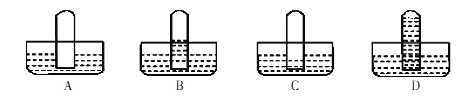
(2)生成白色Fe(OH)2 沉淀的操作是用长滴管吸取不含O2的NaOH 溶液,插入FeSO4溶液液面下,再挤出NaOH 溶液。
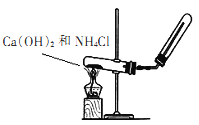
方法二: 如右图装置中,用NaOH 溶液、铁屑、稀H2SO4等试剂制备。
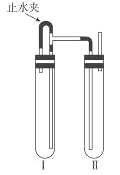
(1)在试管I里加入的试剂是___________。
(2)为了制得白色Fe(OH)2沉淀,在试管I和II中加入试剂,打开止水夹,塞紧塞子后,检验试管II出口处排出的氢气的纯度。当排出的氢气纯净时,再________(如何操作)。这样生成的Fe(OH)2 沉淀能较长时间保持白色。原因是____________。