题目内容
【题目】碳、硫和钒的相关化合物,在药物化学及催化化学等领域应用广泛。回答下列问题:
(1)基态钒的原子结构示意图为____________________________;
(2)VO43-的中心原子价层孤电子对数目为______,一个VO43-离子中含有_______个σ键;
(3)2-巯基烟酸氧钒配合物(图1) 是副作用小的有效调节血糖的新型药物。
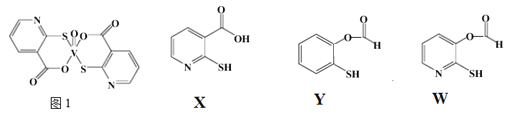
①该药物中N原子的杂化方式是_______;
②X、Y、W三种物质在水中的溶解性由大到小的顺序为________,原因是__________;
已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”(或大π键)。大π键可用![]()
![]() 表示,其中m、n分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为
表示,其中m、n分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为![]()
![]() 。
。
③下列微粒中存在“离域Π键”的是_____;
A.O3 B.SO42- C.H2S D.NO3-
④CS2分子中大π键可以表示为_______________;
(4)偏钒酸铵加热分解生成五氧化二钒、氨气、水。偏钒酸铵的阴离子呈如下图2所示的无限链状结构,则偏钒酸铵的化学式为_________;
(5)某六方硫钒化合物晶体的晶胞如图4所示(![]() 表示V,
表示V,![]() 表示S),该晶胞的化学式为VS。图3 为该晶胞的俯视图。
表示S),该晶胞的化学式为VS。图3 为该晶胞的俯视图。
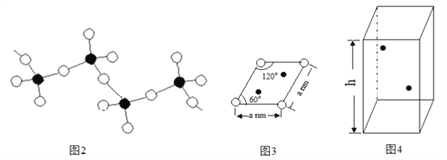
①请在图4中用![]() 标出V原子的位置;
标出V原子的位置;
②已知晶胞的密度为dg/cm3 ,计算晶胞参数h =_____________cm。(列出计算式即可)
【答案】  0 4 sp2 X>W>Y AD X中含有羧基可以与水分子形成氢键,增强水溶性;Y中含有酯基和苯环,W中含有酯基,都不利于水的溶解
0 4 sp2 X>W>Y AD X中含有羧基可以与水分子形成氢键,增强水溶性;Y中含有酯基和苯环,W中含有酯基,都不利于水的溶解 ![]()
![]() NH4VO3 八个顶点各一个,四条棱上各一个 【答题空10】
NH4VO3 八个顶点各一个,四条棱上各一个 【答题空10】![]()
【解析】(1)钒为23号元素,钒的原子结构示意图为: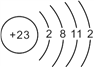 答案为:
答案为:
(2)VO43-的中心原子为V,V最外层有5个电子,V价层孤电子对数目=![]() =0,V周围有4个O与V形成化学键,所以一个VO43-离子中含有4个σ键。答案为: 0 、 4
=0,V周围有4个O与V形成化学键,所以一个VO43-离子中含有4个σ键。答案为: 0 、 4
(3)①该药物中N原子形成2个σ键,1个π键,N的价层电子对=孤对电子+σ键个数=1+2=3,所以N原子采取sp2杂化。②X中含有羧基可以与水分子形成氢键,增强水溶性;Y中含有酯基和苯环,W中含有酯基,都不利于水的溶解,因此X、Y、W三种物质在水中的溶解性由大到小的顺序为:X>W>Y;③从题目表述来看,形成离域Π键的条件是:原子都在同一平面上且这些原子有相互平行的p轨道。根据价层电子对互斥理论,O3为平面三角形,SO42-为正四面体,H2S为角形,NO3-为平面三角形。因此SO42-一定不存在离域Π键,H2S中H原子没有P轨道,也不存在离域Π键,O3和NO3-既是平面形,又有P轨道,可以形成离域Π键。所以选AD. ④CS2是直线型结构,又有P轨道,因此可以形成三中心四电子的离域Π键:![]()
![]() 。答案为:①sp2 ②X>W>Y X中含有羧基可以与水分子形成氢键,增强水溶性,Y中含有酯基和苯环,W中含有酯基,不利于水的溶解③AD
。答案为:①sp2 ②X>W>Y X中含有羧基可以与水分子形成氢键,增强水溶性,Y中含有酯基和苯环,W中含有酯基,不利于水的溶解③AD
④![]()
![]()
(4)由链状结构可知每个V与3个O形成阴离子,且V的化合价为+5价,则偏钒酸铵的化学式为:NH4VO3。答案为:NH4VO3
(5)①该晶胞的化学式为VS,结合该晶胞的俯视图可知,一个该晶胞含有2个V原子2个S原子,因此V原子的位置是:晶胞中八个顶点各一个,四条棱上各一个 。
②因为一个该晶胞中有2个VS,所以一个晶胞质量为2![]() (32+51)/NA,根据图3得到晶胞底面积为:a
(32+51)/NA,根据图3得到晶胞底面积为:a![]() ,所以晶胞的体积为:a
,所以晶胞的体积为:a![]() ,1nm=
,1nm=![]() cm,根据公式ρ=
cm,根据公式ρ=![]() 可得:d=
可得:d=![]() 所以h=
所以h=![]() .答案为:①晶胞中八个顶点各一个,四条棱上各一个②h=
.答案为:①晶胞中八个顶点各一个,四条棱上各一个②h=![]()





