题目内容
【题目】在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:
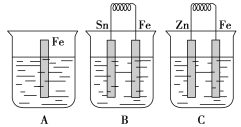
(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________,Sn极附近溶液的pH________(填“增大”、“减小”或“不变”)。C中被腐蚀的金属是________,总反应的离子方程式为________________,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
【答案】(1)Fe+2H+=Fe2++H2↑
(2)2H++2e-=H2↑ 增大
(3)Zn Zn+2H+=Zn2++H2↑ B>A>C
【解析】铁在不同的情况下被腐蚀的速率不同。作原电池的负极时易被腐蚀,作原电池的正极时受到保护不被腐蚀。

练习册系列答案
相关题目
【题目】温度为T时,向4L恒容密闭容器中充入2molPCl5,反应PCl5(g)PCl3(g)+Cl2(g),经一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
A.反应在前50s的平均速率为v(PCl3)=0.0064mol/(Ls)
B.保持其它条件不变,升高温度,平衡时c(PCl3)=0.11mol/L,则反应的△H<0
C.相同温度下,起始时向容器中充入4molPCl3、4molCl2 , 达到平衡时,则此反应的化学平衡常数为0.025mol/L
D.相同温度下,起始时间向容器中充入2molPCl5、0.40molPCl3和0.40molCl2 , 达到平衡前v(正)<v(逆)



