题目内容
14.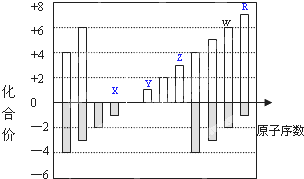 如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )| A. | Y和Z两者最高价氧化物对应的水化物能相互反应 | |
| B. | 气态氢化物的稳定性:W>R | |
| C. | WO3和水反应形成的化合物是离子化合物 | |
| D. | 原子半径:Z>Y>X |
分析 短周期元素,由表中化合价可知,X的化合价为-1价,没有正化合价,故X为F元素,Y的化合价为+1价,处于ⅠA族,原子序数大于F元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R的最高正价为+7价,应为Cl元素,以此解答该题.
解答 解:短周期元素,由表中化合价可知,X的化合价为-1价,没有正化合价,故X为F元素,Y的化合价为+1价,处于ⅠA族,原子序数大于F元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R的最高正价为+7价,应为Cl元素,
A.Y和Z两者最高价氧化物对应的水化物分别为氢氧化钠、氢氧化铝,氢氧化铝具有两性,可与氢氧化钠反应,故A正确;
B.W为S,R为Cl,所以非金属性Cl>S,则气态氢化物的稳定性HCl>H2S,故B错误;
C.SO3和水反应形成的化合物为硫酸,为共价化合物,故C错误;
D.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Al>F,故D错误.
故选A.
点评 本题考查结构性质与位置关系应用,难度不大,掌握化合价与族序数关系是推断元素解题的关键.

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
4.W、X、Y、Z四种短周期元素在周期表中的相对位置如图所示,W的气态氢化物可与Z的气态氢化物反应生成离子化合物,由此可知( )
| W | X | |
| Y | Z |
| A. | X、Y、Z中最简单氢化物稳定性最差的是Y | |
| B. | X元素形成的单核阴离子还原性强于Y | |
| C. | Z元素氧化物对应水化物的酸性强于Y | |
| D. | Y元素单质在化学反应中只表现出氧化性 |
5.下列排列顺序正确的是( )
| A. | 微粒半径:Mg2+>F- | B. | 稳定性:HI>HBr | ||
| C. | 酸性:H2CO3>H3PO4 | D. | 熔点:Al>Na |
19.现代化学键理论认为苯环结构中不存在单双键交替结构,可以作为证据的事实是( )
①苯不能使KMnO4溶液褪色
②苯中碳碳键的键能均相等
③苯能在一定条件下跟H2加成生成环己烷
④经实验测得邻二甲苯仅一种结构
⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不因化学变化而使溴水褪色.
①苯不能使KMnO4溶液褪色
②苯中碳碳键的键能均相等
③苯能在一定条件下跟H2加成生成环己烷
④经实验测得邻二甲苯仅一种结构
⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不因化学变化而使溴水褪色.
| A. | ②③④⑤ | B. | ①③④⑤ | C. | ①②③④ | D. | ①②④⑤ |
6.已知下述三个实验中的物质均能发生化学反应.
下列判断正确的是( )
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铁钉放入氯化铁溶液中 |
| A. | 实验①和③中的铁钉只作还原剂 | |
| B. | 实验③中反应的离子方程式为Fe+Fe3+═2Fe2+ | |
| C. | 实验②中Fe2+既显氧化性又显还原性 | |
| D. | 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ |
3.从海水中可以提取溴,但得到的液溴中常常溶有少量氯气,除去氯气应该采用的方法有( )
| A. | 加入适量的FeCl2溶液 | B. | 加入适量的KBr溶液 | ||
| C. | 加入适量的饱和食盐水 | D. | 加入适量的Na2S溶液 |
4.下列是有关外界条件对化学反应速率和化学平衡影响的图象,其中图象和实验结论表达均正确的是( )


| A. | ①是其他条件一定时,反应速率随温度变化的图象,则正反应△H>0 | |
| B. | ②是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图象 | |
| C. | ③是在有无催化剂存在条件下,建立平衡过程的图象,a是使用催化剂时的曲线 | |
| D. | ④是一定条件下,向含有一定量A的恒容密闭容器中逐渐加入B,达平衡时A的转化率的图象 |
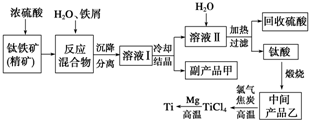 金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.