题目内容
分别将下列物质滴入苯酚溶液中,产生白色沉淀的是
- A.浓溴水
- B.氢氧化钠溶液
- C.稀盐酸
- D.氯化铁溶液
考查苯酚的化学性质。苯酚俗称石炭酸,和氢氧化钠反应,但不会产生白色沉淀。和氯化铁也发生显色反应,溶液显紫色。和盐酸不反应,只有和浓溴水反应生成2,4,6-三溴苯酚白色沉淀,答案选A。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案| A、滴定管在使用前要用待装液润洗,而容量瓶不用润洗 | B、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | C、检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 | D、将CO2和SO2混合气体分别通入BaCl2溶液、Ba(NO3)2溶液中,最终都有沉淀生成 |
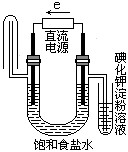
苯酚具有弱酸性,在空气中易被氧化。工业上以苯、硫酸、氢氧化钠、亚硫酸钠为原料合成苯酚的方法可简单表示为:

(1)根据上述反应判断下列三种物质的酸性由强到弱的顺序为 (填序号)。
A.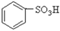 B.
B. C.H2SO3
C.H2SO3
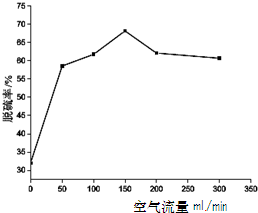
(2)步骤④与使用CO2相比,使用SO2的优点是 (答一个方面)。
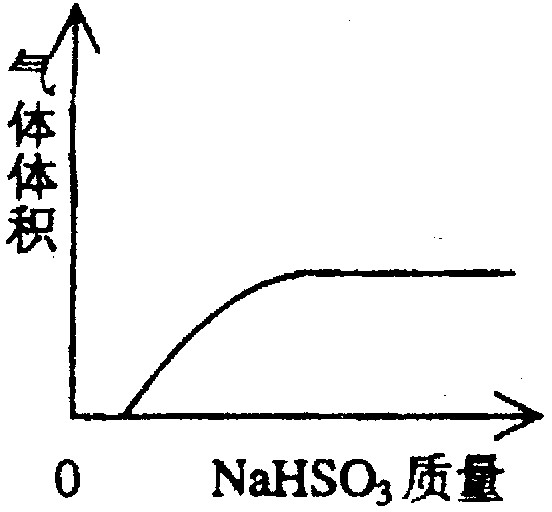
(3)经反应④得到的产物除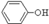 外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在
外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在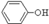 、SO32-、HSO3-,写出实验步骤、预期现象和结论。
、SO32-、HSO3-,写出实验步骤、预期现象和结论。
限选仪器及试剂:试管、滴管、玻璃棒、过滤装置和滤纸;2mol·L-1盐酸、1mol·L-1 BaCl2溶液、品红溶液、0.01 mol·L-1酸性KMnO4溶液、1 mol·L-1 FeCl3溶液、饱和溴水等。
|
实验步骤 |
预期现象和结论 |
|
步骤1:取少量待测液于试管中,加入足量的1 mol·L-1BaCl2溶液,静置、过滤,得滤液和沉淀。将滤液分置于试管A、B中,沉淀置于试管C中。 |
|
|
步骤2:往试管A中加入 。 |
,说明溶液中含有HSO3-。 |
|
步骤3:往试管B中加入 。 |
。 |
|
步骤4:往试管C中加入2 mol·L-1盐酸酸化,再滴入1~2滴品红溶液。 |
,说明溶液中含有SO32-。 |
(4)纯度测定:称取1.00g产品溶解于足量温水中,向其中加入足量饱和溴水(产品中除苯酚外,不含其它与饱和溴水反应生成沉淀的物质),苯酚全部生成三溴苯酚沉淀,经过滤、洗涤、干燥后,称得沉淀质量为3.31g,则产品中苯酚的质量分数为 。(苯酚的分子式为C6H6O,三溴苯酚的分子式为C6H3Br3O,它们的相对分子质量分别为94、331)



 B、
B、
 D、
D、