题目内容
雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为 。
(2)上述反应中的氧化剂是 ,反应产生的气体可用 吸收。
(3)As2S3和HNO3有如下反应:
As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O若生成2 mol H3 AsO4,则反应中转移电子的物质的量为 。若将该反应设计成一原电池,则NO2应该在 (填“正极”或“负极”)附近逸出。
(4)若反应产物NO2和11.2 L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量 (选填编号)。
a.小于0.5 mol b.等于0.5 mol
c.大于0.5 mol d.无法确定
(1)1∶1
(2)As2S3 氢氧化钠溶液(或硫酸铜溶液)
(3)10 mol 正极
(4)a
【解析】(1)As在As2S3中的化合价为+3,在As4S4中的化合价为+2,每摩As2S3转化为As4S4时得到2 mol e-,而每摩SnCl2转化为SnCl4时失去2 mol e-,故二者在反应时物质的量之比为1∶1。(2)H2S既可与NaOH溶液反应,又能与CuSO4溶液反应。(3)当生成2 mol H3AsO4时,同时生成了3 mol S,二者共失去电子10 mol。HNO3在反应中作氧化剂,在正极上发生反应,所以NO2应在正极上生成。(4)根据反应4NO2+O2+2H2O=4HNO3可知,反应共生成2 mol HNO3,浓HNO3与碳反应时的物质的量之比为4∶1,所以2 mol HNO3如完全反应可生成CO2 0.5 mol。但由于硝酸的浓度降低到一定程度时,碳就不再与硝酸反应,所以实际产生CO2的物质的量应小于0.5 mol。

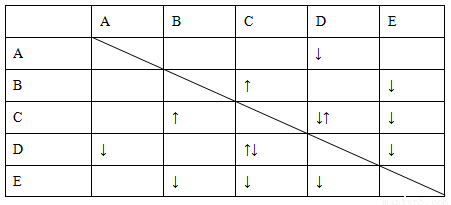
根据表中信息判断,下列选项不正确的是 ( )。
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4…… |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO4-…… | Cl2、Mn2+…… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱的顺序为MnO4->Cl2>Fe3+>Br2