题目内容
【题目】温度为T时,向![]() 恒容密闭容器中充入
恒容密闭容器中充入![]()
![]() ,反应
,反应![]() 经过一段时间后达到平衡。反应过程中测定的部分数据见表:下列说法正确的是
经过一段时间后达到平衡。反应过程中测定的部分数据见表:下列说法正确的是![]()
| 0 | 50 | 150 | 250 | 350 |
| 0 |
|
|
|
|
A.反应在前50s的平均速率![]()
![]()
B.保持其他条件不变,升高温度,平衡时![]()
![]() ,则反应的
,则反应的![]()
C.相同温度下,起始时向容器中充入![]() mol
mol![]() 、
、![]() mol
mol![]() 和
和![]() mol
mol![]() ,反应达到平衡前
,反应达到平衡前![]() 正
正![]() 逆
逆![]()
D.相同温度下,起始时向容器中充入![]() mol
mol![]() 和
和![]() mol
mol![]() ,达到平衡时,
,达到平衡时,![]() 的转化率小于
的转化率小于![]()
【答案】C
【解析】
A.结合![]() 计算反应在前50s的平均速率为v(PCl3);
计算反应在前50s的平均速率为v(PCl3);
B.由表格数据可知,250s达到平衡,利用平衡数据计算平衡前后![]() 的浓度变化判断平衡移动方向;
的浓度变化判断平衡移动方向;
C.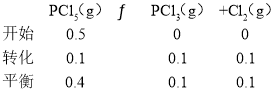 ,
,![]() ,起始时向容器中充入1.0 molPCl5、0.20 molPCl3和0.20 molCl2,
,起始时向容器中充入1.0 molPCl5、0.20 molPCl3和0.20 molCl2,![]() ;
;
D.等效为起始加入1.0molPCl5,与原平衡相比,压强增大,平衡向逆反应方向移动。
A.由表中数据可知,50s内![]() ,
,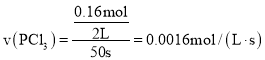 ,故A错误;
,故A错误;
B.由表中数据可知,平衡时![]() ,保持其他条件不变,升高温度,平衡时,
,保持其他条件不变,升高温度,平衡时,![]() ,则
,则![]() ,说明升高温度平衡正向移动,正反应为吸热反应,即
,说明升高温度平衡正向移动,正反应为吸热反应,即![]() ,故B错误;
,故B错误;
C.250s处于平衡状态,则:平衡常数![]() ,
,
起始时向容器中充入![]() 、
、![]() 和
和![]() ,起始时
,起始时![]() 的浓度为
的浓度为![]() 、
、![]() 的浓度为
的浓度为![]() 、
、![]() 的浓度为
的浓度为![]() ,浓度商
,浓度商![]() ,说明平衡向正反应方向移动,反应达平衡前
,说明平衡向正反应方向移动,反应达平衡前![]() 正
正![]() 逆
逆![]() ,故C正确;
,故C正确;
D.相同温度下,起始时向容器中充入 ![]() mol
mol ![]() 和
和 ![]() mol
mol ![]() ,
,![]() 等效为起始加入
等效为起始加入![]() ,达到平衡时,
,达到平衡时,![]() 的物质的量等于
的物质的量等于![]() ,平衡时
,平衡时![]() 的转化率
的转化率![]() ,故D错误;
,故D错误;
故选C。

【题目】根据图1、图2、图3及题中信息,回答下列问题
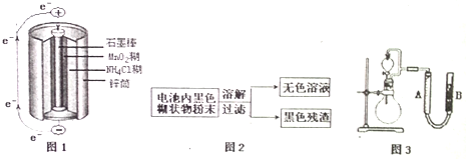
![]() 图1是锌锰干电池基本构造图,该电池的负极材料是 ______ ;工作时
图1是锌锰干电池基本构造图,该电池的负极材料是 ______ ;工作时![]() 离子在正极放电产生两种气体,其中一种气体分子是含
离子在正极放电产生两种气体,其中一种气体分子是含![]() 的微粒,正极的电极反应式是 ______ ;当电路中每通过
的微粒,正极的电极反应式是 ______ ;当电路中每通过![]() ,负极质量减少 ______ ;
,负极质量减少 ______ ;
![]() 图2是利用废旧锌锰干电池内的黑色糊状物分离得到黑色残渣
图2是利用废旧锌锰干电池内的黑色糊状物分离得到黑色残渣![]() 的流程图.该流程中溶解和过滤操作均要使用到的玻璃仪器有 ______ ;
的流程图.该流程中溶解和过滤操作均要使用到的玻璃仪器有 ______ ;
![]() 图3是探究
图3是探究![]() 在制
在制![]() 过程中的作用的实验装置图,利用该装置完成下表中实验一和实验二,实验过程中有关实验现象和所得数据如下表
过程中的作用的实验装置图,利用该装置完成下表中实验一和实验二,实验过程中有关实验现象和所得数据如下表![]() 已知:两次实验气体的体积在相同条件下测定:
已知:两次实验气体的体积在相同条件下测定:![]() 由分液漏斗滴入到圆底烧瓶
由分液漏斗滴入到圆底烧瓶![]() 。
。
序号 | 烧瓶中的物质 | 实验记录 | 实验结论 |
实验一 | 足量 |
|
|
实验二 |
|
|
|
![]() 在测量气体体积时,除要注意待气体温度恢复至室温、平视度数外,还需要注意 ______ ;
在测量气体体积时,除要注意待气体温度恢复至室温、平视度数外,还需要注意 ______ ;
![]() 实验一、二中参加反应的
实验一、二中参加反应的![]() 的物质的量之比为 ______ 。
的物质的量之比为 ______ 。