题目内容
【题目】聚芳酯(PAR)是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域应用广泛。下图是利用乙酰丙酸(![]() )合成聚芳酯E的路线(省略部分产物):
)合成聚芳酯E的路线(省略部分产物):

已知:![]()
![]() ,(R、R′表示烃基)
,(R、R′表示烃基)
(1)A中含有的官能团是_______________(填官能团名称)。
(2)B与D的反应类型为_______________,B的结构简式为______________________
(3)C生成D的反应化学方程式为______________________。
(4)C分子的核磁共振氢谱中有_________个吸收峰;同时符合下列要求的C的同分异构体有_______种。①能发生银镜反应 ②能与NaHCO3溶液反应 ③遇FeCl3溶液显紫色
F与C属于官能团异构的同分异构体,且只含一种官能团,则1mol F与足量NaOH溶液反应时消耗NaOH的物质的量为_____________
(5)根据合成聚芳酯E的路线,请你以苯酚及2-丙醇为原料(无机试剂任选),设计合成G: 的路线。___________
的路线。___________
【答案】羟基、羧基 缩聚反应 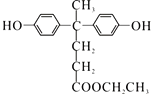
 +2SOCl2→
+2SOCl2→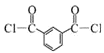 +2SO2+2HCl 4 10 4mol
+2SO2+2HCl 4 10 4mol 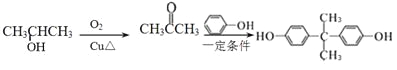
【解析】
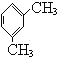 被酸性高锰酸钾氧化生成的C为
被酸性高锰酸钾氧化生成的C为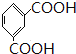 ,C中羧基上的羟基被氯原子取代生成的D为
,C中羧基上的羟基被氯原子取代生成的D为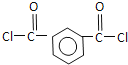 ,由聚芳酯E的结构简式可知B的结构简式为
,由聚芳酯E的结构简式可知B的结构简式为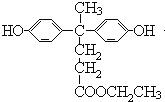 ,A的分子式为C17H18O4,A与CH3CH2OH反应生成B,则A的结构简式为
,A的分子式为C17H18O4,A与CH3CH2OH反应生成B,则A的结构简式为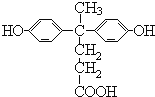 。
。
 被酸性高锰酸钾氧化生成的C为
被酸性高锰酸钾氧化生成的C为 ,C中羧基上的羟基被氯原子取代生成的D为
,C中羧基上的羟基被氯原子取代生成的D为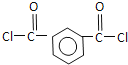 ,由聚芳酯E的结构简式可知B的结构简式为
,由聚芳酯E的结构简式可知B的结构简式为 ,A的分子式为C17H18O4,A与CH3CH2OH反应生成B,则A的结构简式为
,A的分子式为C17H18O4,A与CH3CH2OH反应生成B,则A的结构简式为 。
。
(1)A的结构简式为 ,含有的官能团是:羧基、羟基;
,含有的官能团是:羧基、羟基;
(2)B与D的反应类型为缩聚反应,B的结构简式为 ;
;
(3)根据以上分析可知C生成D的反应化学方程式为: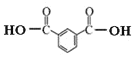 +2SOCl2→
+2SOCl2→ 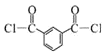 +2SO2+2HCl;
+2SO2+2HCl;
(4)C的结构简式为 ,因此核磁共振氢谱中有4个吸收峰;同时符合下列要求的C的同分异构体:①能发生银镜反应,说明含有醛基,②能与NaHCO3溶液反应,说明含有羧基,③遇FeCl3溶液显紫色,说明含有酚羟基,则取代基为-OH、-COOH、-CHO,当-OH、-COOH处于邻位时,-CHO有4种位置,当-OH、-COOH处于间位时,-CHO有4种位置,当-OH、-COOH处于对位时,-CHO有2种位置,共有10种;F与C属于官能团异构的同分异构体,且只含一种官能团,则F为
,因此核磁共振氢谱中有4个吸收峰;同时符合下列要求的C的同分异构体:①能发生银镜反应,说明含有醛基,②能与NaHCO3溶液反应,说明含有羧基,③遇FeCl3溶液显紫色,说明含有酚羟基,则取代基为-OH、-COOH、-CHO,当-OH、-COOH处于邻位时,-CHO有4种位置,当-OH、-COOH处于间位时,-CHO有4种位置,当-OH、-COOH处于对位时,-CHO有2种位置,共有10种;F与C属于官能团异构的同分异构体,且只含一种官能团,则F为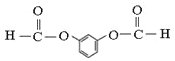 ,1mol F与足量NaOH溶液反应时消耗NaOH的物质的量为4mol;
,1mol F与足量NaOH溶液反应时消耗NaOH的物质的量为4mol;
(5)结合转化关系中![]() 与苯酚转化为A的反应可知,2-丙醇催化氧化生成丙酮
与苯酚转化为A的反应可知,2-丙醇催化氧化生成丙酮![]() ,丙酮与苯酚反应得到
,丙酮与苯酚反应得到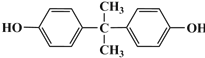 ,因此合成路线流程图可设计为:
,因此合成路线流程图可设计为: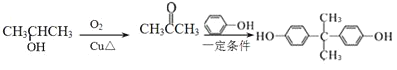 。
。

【题目】下列生产或实验事实引出的相应结论不正确的是( )
选项 | 事实 | 结论 |
A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间变短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
B | 工业制硫酸中,在SO3的吸收阶段,吸收塔里要装填瓷环 | 增大气液接触面积,使SO3的吸收速率增大 |
C | 在容积可变的密闭容器中发生反应:2NH3(g) | 正反应速率加快,逆反应速率减慢 |
D | A、B两支试管中分别加入等体积5%的H2O2,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
A. A B. B C. C D. D