题目内容
【题目】已知HF分子在一定条件下会发生二聚反应:2HF(g)(HF)2(g)。经实验测得,不同压强下,体系的平均相对分子质量(M=![]() )随温度(T)的变化曲线如图所示,下列说法正确的是( )
)随温度(T)的变化曲线如图所示,下列说法正确的是( )
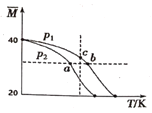
A.该反应的ΔH>0B.气体的压强:p(a)>p(b)=p(c)
C.平衡常数:K(a)=K(b)<K(c)D.测定HF的相对分子质量要在低压、高温条件下
【答案】D
【解析】
A.温度升高平均摩尔质量减小,气体质量守恒,物质的量增大,说明平衡逆反应方向进行,升温平衡向吸热反应方向进行,正反应是放热反应,△H<0,故A错误;
B.b、c点是压强相同条件下的化学平衡,依据图象分析可知温度不变时,增大压强,气体物质的量减小,气体摩尔质量越大,p1>p2,气体的压强:p(a)<p(b)=p(c),故B错误;
C.平衡常数随温度变化不随压强变化,a、b、c点的温度不同,正反应是放热反应,温度越高平衡常数越小,平衡常数:K(a)>K(c)>K(b),故C错误;
D.反应是气体体积减小的放热反应,测定HF的相对分子质量应使平衡逆向进行,需要在低压高温条件下进行提高HF的纯度,故D正确;
答案选D。

 阅读快车系列答案
阅读快车系列答案【题目】下列实验中的颜色变化,与氧化还原反应无关的是
A | B | C | D | |
实验 | NaOH溶液滴入FeSO4溶液中 | 石蕊溶液滴入氯水中 | Na2S溶液滴入AgCl浊液中 | 热铜丝插入稀硝酸中 |
现象 | 产生白色沉淀,随后变为红褐色 | 溶液变红,随后迅速褪色 | 沉淀由白色逐渐变为黑色 | 产生无色气体,随后变为红棕色 |
A. A B. B C. C D. D
【题目】2019年12月中旬以来,新型冠状病毒肺炎(NCP)肆虐全球,酒精、84消毒液、双氧水、过氧乙酸等化学品是常用的消毒剂,能够杀死新型冠状病毒。
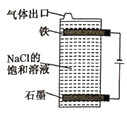
Ⅰ.如图是简易84消毒液发生器,写出该电解池中发生的总反应的化学方程式:__。
Ⅱ.过氧化尿素是一种新型漂白剂、消毒剂,漂白、消毒的效果优于H2O2和过氧乙酸。
某工业用过氧化尿素的部分参数见下表:
分子式 | 外观 | 热分解温度 | 熔点 | 水溶性(20℃) |
CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 500g·L-1 |
合成过氧化尿素的流程及反应器的示意图如图:

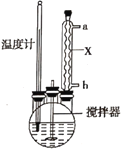
回答下列问题:
(1)流程中操作①的名称为__,仪器X的名称是__。
(2)流程中操作②的具体过程是__。
A.盐析、过滤 B.减压蒸馏、结晶、过滤 C.分液、过滤 D.常压蒸馏、萃取
(3)搅拌器选用的材质是玻璃而不是铁质的原因是__。
(4)为测定产品中活性氧的含量(含双氧水34%,则其中活性氧为16%),一般采用KMnO4标准溶液进行滴定,但由于KMnO4的强氧化性,其溶液很容易被空气或水中的少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液有如下步骤:
a.利用氧化还原滴定方法,在70~80℃条件下用基准试剂纯度高、相对分子质量较大、稳定性较好的物质)溶液标定其浓度。
b.过滤得到的KMnO4溶液贮存于棕色试剂瓶中并放在暗处。
c.称取稍多于所需量的KMnO4固体溶于水中,将溶液加热并保持微沸![]() 。
。
d.用微孔玻璃漏斗过滤除去难溶的MnO(OH)2。
①请按照正确的流程对上述步骤进行排序__(填字母)。
②在下列物质中,用于标定KMnO4溶液的基准试剂最好选用__。
A.H2C2O4·2H2O B.FeSO4 C.浓盐酸 D.Na2SO3
③若准确称取Wg你选的基准试剂溶于水配成500mL溶液,取25.00mL置于锥形瓶中,用KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。称取干燥样品1.2g,溶解后置于锥形瓶中加入1mL6mol·L-1的硫酸,然后用上述KMnO4标准溶液滴定(KMnO4溶液与尿素不反应),平行实验三次,实验结果如下:
实验序号 | 1 | 2 | 3 | |
KMnO4溶液体积 (mL) | 滴定前读数 | 0.00 | 0.00 | 1.00 |
滴定后读数 | 19.90 | 22.70 | 21.10 |
产品中活性氧的质量分数为__(用含字母的最简等式表示)。