��Ŀ����
����Ŀ����14�֣�
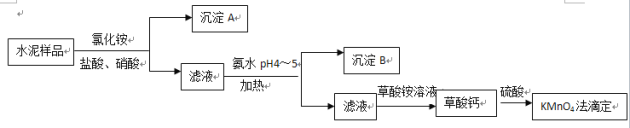
ˮ������Ҫ�Ľ������ϡ�ˮ�����ϵ���Ҫ�ɷ�ΪCaO��SiO2��������һ��������������þ�Ƚ����������ʵ���Ҳⶨˮ����Ʒ�иƺ����Ĺ�����ͼ��ʾ��
�ش��������⣺
��1���ڷֽ�ˮ����Ʒ�����У�������Ϊ�ܼ����Ȼ��Ϊ���ܼ���������뼸�����ᡣ���������Ŀ����__________������ʹ��___________�������ᡣ
��2������A����Ҫ�ɷ���_________���䲻����ǿ�ᵫ����һ�����ᷴӦ���÷�Ӧ�Ļ�ѧ����ʽΪ____________________________________��
��3���Ӱ�ˮ�����м��ȵ�Ŀ����___________������B����Ҫ�ɷ�Ϊ_____________��____________���ѧʽ����
��4������Ƴ�����ϡH2SO4��������KMnO4����Һ�ζ���ͨ���ⶨ��������ɼ�ӻ�֪�Ƶĺ������ζ���ӦΪ��![]() +H++H2C2O4��Mn2++CO2+H2O��ʵ���г�ȡ0.400 gˮ����Ʒ���ζ�ʱ������0.0500 mol��L-1��KMnO4��Һ36.00 mL�����ˮ����Ʒ�иƵ���������Ϊ______________��
+H++H2C2O4��Mn2++CO2+H2O��ʵ���г�ȡ0.400 gˮ����Ʒ���ζ�ʱ������0.0500 mol��L-1��KMnO4��Һ36.00 mL�����ˮ����Ʒ�иƵ���������Ϊ______________��
���𰸡�
��1������Ʒ�п��ܴ��ڵ�Fe2+����ΪFe3+ �� ˫��ˮ(H2O2)
��2�� SiO2 (��H2SiO3)��SiO2+4HF![]() SiF4��+2H2O
SiF4��+2H2O
��3����ֹ�������ɣ��׳���������Fe(OH)3 �� ![]() (OH)3
(OH)3
��4�� 5Ca2+��5H2C2O4��2KMnO4
n(KMnO4)=0.0500mol/L��36.00��10��3mL=1.80��10��3mol
n(Ca2+)=4.50��10��3mol
ˮ���иƵ���������Ϊ4.50��10��3mol��40.0g/mol/0.400g��100%=45.0%
��������
��1�� Fe3+������pH��Сʱת��Ϊ������������Ҫ��Fe2+����ΪFe3+ ��
˫��ˮ���Խ�Fe2+����ΪFe3+�Ҳ����������ʡ�
��2�� �������費����һ������Һ�����Գ���A�Ƕ������衣
SiO2+4HF![]() SiF4��+2H2O
SiF4��+2H2O
��3�����ȿ��Դٽ�Fe3+��Al3+ˮ��ת��ΪFe(OH)3��![]() (OH)3��
(OH)3��
pH4��5ʱCa2+��Mg2+��������Fe3+��Al3+���������Գ���BΪFe(OH)3��![]() (OH)3��
(OH)3��
��4�� 5Ca2+��5H2C2O4��2KMnO4
n(KMnO4)=0.0500mol/L��36.00��10��3mL=1.80��10��3mol
n(Ca2+)=4.50��10��3mol
ˮ���иƵ���������Ϊ4.50��10��3mol��40.0g/mol/0.400g��100%=45.0%��


