题目内容
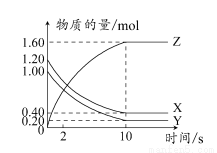
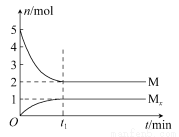
向某密闭容器中加入0.15 mol/L A、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图中甲图所示[t0时c(B)未画出,t1时增大到0.05 mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
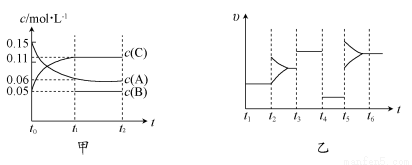
(1)若t4时改变的条件为减小压强,则B的起始物质的量浓度为_____mol/L。
(2)若t5时改变的条件是升温,此时v(正)>v(逆),若A的物质的量减少0.03 mol时,容器与外界的热交换总量为akJ,写出该反应的热化学方程式_______。
(3)若t1=15s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______ mol/L,A的转化率为________。
(4)t3时改变的某一反应条件可能是________(选填序号)。
a.使用催化剂
b.增大压强
c.增大反应物浓度
(1)0.02
(2)3A(g) 2C(g)+B(g) ΔH=+100a kJ·mol-1
2C(g)+B(g) ΔH=+100a kJ·mol-1
(3)0.004 60% (4)a、b
【解析】这是一道反应速率及其影响因素与平衡移动的综合性题目。
(1)t4时,减小压强,v(正)、v(逆)以同等倍数下降,说明反应前后化学计量数之和相等,由A、C浓度变化曲线知,到t1时,A、C的浓度变化量为Δc(A)=0.15-0.06=0.09(mol·L-1),Δc(C)=0.11-0.05=0.06(mol·L-1),即A、C的化学计量数之比为0.09∶0.06=3∶2,故反应式为3A(g) 2C(g)+B(g),则B的起始浓度为0.05-0.03=0.02(mol·L-1)。
2C(g)+B(g),则B的起始浓度为0.05-0.03=0.02(mol·L-1)。
(2)因升温,v(正)>v(逆),平衡正向进行,故此反应为吸热反应,其热化学反应方程式为3A(g) 2C(g)+B(g)
2C(g)+B(g)
ΔH=+100a kJ·mol-1。
(3)v(C)= 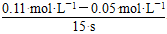 =0.004 mol·L-1·s-1
=0.004 mol·L-1·s-1
α(A)= 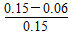 ×100%=60%。
×100%=60%。
(4)乙图中t3时刻v(正)、v(逆)以同等倍数增大,故应是增大压强或加入催化剂。