题目内容
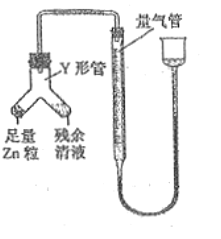
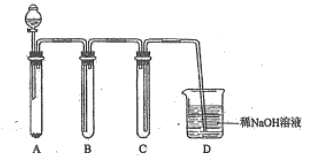
【题目】实验室用废铜屑和稀硝酸反应制备无水硝酸铜,下列装置能达到实验目的的是( )
A. 制备硝酸铜溶液 B. 吸收尾气
B. 吸收尾气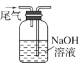 C. 加热蒸干
C. 加热蒸干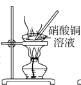 D. 脱去结晶水
D. 脱去结晶水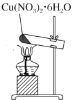
【答案】A
【解析】
A.稀硝酸与铜反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,仪器装置完全正确,加热能加快反应速率,能够制得硝酸铜溶液,A项正确;
B.广口瓶内进气导管口应在液面下,出气导管口应与橡胶塞平齐,另外,NO气体不能被NaOH完全吸收,B项错误;
C.硝酸铜在水溶液中能发生水解反应:Cu(NO3)2+2H2O![]() Cu(OH)2+2HNO3,加热硝酸铜溶液时因水解反应吸热且HNO3随着水分挥发,促使水解平衡向正反应方向移动,直到水解完全,无法到Cu(NO3)2·6H2O晶体,C项错误;
Cu(OH)2+2HNO3,加热硝酸铜溶液时因水解反应吸热且HNO3随着水分挥发,促使水解平衡向正反应方向移动,直到水解完全,无法到Cu(NO3)2·6H2O晶体,C项错误;
D.加热固体应在坩埚内,另外,加热Cu(NO3)2·6H2O晶体时发生水解反应,蒸干水解完全,得不到无水硝酸铜,D项错误;答案选A。

练习册系列答案
相关题目