题目内容
【题目】室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是( )
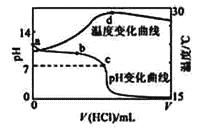
A. a点由水电离出的c(H+)=1.0×10-14mol/L
B. b点:c(NH4+)+c(NH3·H2O) > c(Cl-)
C. c点:反应消耗的HCl 和NH3·H2O 的关系为:n(HCl)= n(NH3·H2O)
D. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
【答案】B
【解析】试题分析:A、因a点7<pH<14,因此水电离出的c(H+)>1.0×10-14molL-1,故A错误;B、b点时pH>7,则盐酸和氨水反应,氨水过量,则c(NH4+)+c(NH3H2O)>c(Cl-),故B正确;C、氯化铵水溶液显酸性,c点pH=7溶液呈中性,故n(HCl)<n(NH3·H2O) ,故C错误;D、d点时盐酸和氨水恰好完全反应,放热最多,再加盐酸温度降低只能是加入盐酸的温度低于溶液温度,这才是温度下降的原因,故D错误;

【题目】一定温度下,难溶强电解质的饱和溶液中存在着沉淀溶解平衡,其平衡常数为
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp(25℃) | 8.0×10﹣16 | 2.2×10﹣20 | 4.0×10﹣38 |
对于含Fe2(SO4)3、FeSO4和CuSO4各0.5mol的混合溶液1L,根据上表数据判断,说法错误的是
A. 向混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
B. 向溶液中加入双氧水,并用CuO粉末调pH,过滤后可获较纯净的CuSO4溶液
C. 该溶液中一定有c(SO42﹣)∶[c(Fe3+)+c(Fe2+)+c(Cu2+)]=5∶4
D. 将少量FeCl3粉末加入含Cu(OH)2的悬浊液中,其中c(Cu2+)增大