题目内容
【题目】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:
2NO2(g)(红棕色)![]() N2O4(g)(无色),如图所示.
N2O4(g)(无色),如图所示.
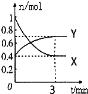
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(Ls),乙中v(N2O4)=6mol/(Lmin),则 中反应更快.
(4)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
【答案】(1)X;(2)减慢;(3)甲;(4)BCF。
【解析】
试题分析:(1)由方程式2NO2(g)(红棕色)![]() N2O4(g)(无色),可知反应中方程式的系数变化较大是NO2;
N2O4(g)(无色),可知反应中方程式的系数变化较大是NO2;
NO2的物质的量变化较大,则X表示NO2的物质的量随时间的变化曲线;(2)温度降低,正逆反应速率都减慢,所以逆反应速率减慢;(3)分别测得甲中v(NO2)=0.3mol/(Ls),乙中v(N2O4)==6mol/(Lmin),v(NO2)=2 v(N2O4)=0.6molL-1min-1=0.01mol/(Ls),则甲反应较快;(4)A.v(NO2)=2v(N2O4),未体现正与逆的关系,不能确定反应是否达到化学平衡状态,错误;B.该反应是反应前后气体体积改变的反应,若容器内压强不再发生变化,说明达平衡状态,正确;C.X的体积分数不再发生变化,说明达平衡状态,正确;D.容器内气体原子总数不再发生变化,从反应发生容器中原子总数就不变,所以不能作平衡状态的标志,错误;E.只要反应发生就符合相同时间内消耗n mol的Y的同时生成2n mol的X,所以不一定达平衡状态,错误;F.相同时间内消耗n mol的Y的同时消耗2n mol的X,说明达平衡状态,正确。

【题目】Ⅰ、用下图所示装置进行实验,将A逐滴加入B中:
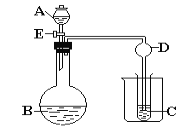
(1)若B为CaCO3,C为C6H5ONa溶液,实验观察到小试管内溶液变浑浊,则酸A比碳酸的酸性_____(填强、弱)。然后往烧杯中加入沸水,可观察到试管C中的现象是____________。
(2)若A是浓氨水,B是生石灰,实验中观察到C溶液先形成沉淀,然后沉淀溶解,当溶液恰好澄清时,关闭E,然后向烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则C是葡萄糖与_____(写化学式)的混合液,仪器D在此实验中的作用是_____________。
Ⅱ、正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。
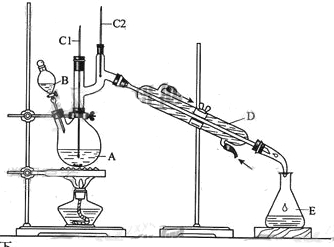
发生的反应如下: CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90—95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中? (填“能”或“不能”),请说明理由 。
(2)加入沸石的作用是 。若加热后发现未加沸石,应采取的正确方法是 。
(3)上述装置图中,B仪器的名称是 ,D仪器的名称是 。
(4)分液漏斗使用前必须进行的操作是 (填正确答案标号)。
A.润湿 B.干燥 C.检漏 D.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在 层(填“上”或“下”)。
(6)反应温度应保持在90—95℃,其原因是 。
(7)本实验中,正丁醛的产率为 %。
【题目】已知25℃ Ksp(Ag2S)=6.3×10-50、Ksp(AgCl)=1.5×10-16。沙市中学某研究性学习小组探究
AgCl、Ag2S沉淀转化的原因。
步 骤 | 现 象 |
Ⅰ.将NaCl与AgNO3溶液混合 | 产生白色沉淀 |
Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
Ⅲ.滤出黑色沉淀,加入NaCl溶液 | 较长时间后,沉淀变为乳白色 |
(1)Ⅰ中的白色沉淀是 。
(2)Ⅱ中能说明沉淀变黑的的离子方程式是 ,沉淀转化的主要原因是 。
(3)滤出步骤Ⅲ中乳白色沉淀,推测含有AgCl。用浓HNO3溶解,产生红棕色气体,部分沉淀未溶
解,过滤得到滤液X和白色沉淀Y。
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀
ⅱ.向Y中滴加KI溶液,产生黄色沉淀
①由ⅰ判断,滤液X中被检出的离子是 。
②由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有AgCl和另一种沉淀_____ _。
(4)该学生通过如下对照实验确认了步骤Ⅲ中 乳白色沉淀产生的原因:在NaCl存在下,氧气将Ⅲ中黑色沉淀氧化。

现 象 | B:一段时间后,出现乳白色沉淀 |
C:一段时间后,无明显变化 |
①A中产生的气体是_________。
②C中盛放的物质W是_________。
③该同学认为B中产生沉淀的反应如下(请补充完整):
2Ag2S + ![]() +
+ ![]() + 2H2O
+ 2H2O ![]() 4AgCl +
4AgCl + ![]() + 4NaOH
+ 4NaOH
④从平衡移动的角度,解释B中NaCl的作用: 。