��Ŀ����
����Ŀ��ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A����һ��ֲ���������ڼ���A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ�����Т٢ڢ�����ͬ�ַ�Ӧ���͡�������ͼ�ش��������⣺

��1��д��A��B��C��D�Ľṹ��ʽ��
A________��B________��C________��D________��
��2��д����������������Ӧ�Ļ�ѧ����ʽ����ע����Ӧ����
____________________����Ӧ����________��
____________________����Ӧ����________��
____________________����Ӧ����________��
��____________________����Ӧ����________��
��4����A��ȼ�շ�Ӧ����ʽ___________________________
���𰸡���1��CH2===CH2��CH3CH3��CH3CH2Cl��CH3CH2OH��
��2�� CH2===CH2+H2![]() CH3CH3���ӳɷ�Ӧ��
CH3CH3���ӳɷ�Ӧ��
CH2==CH2��HCl![]() CH3CH2Cl���ӳɷ�Ӧ��
CH3CH2Cl���ӳɷ�Ӧ��
CH2==CH2��H2O![]() CH3CH2OH���ӳɷ�Ӧ��
CH3CH2OH���ӳɷ�Ӧ��
��CH3CH3��Cl2![]() CH3CH2Cl��HCl��ȡ����Ӧ��
CH3CH2Cl��HCl��ȡ����Ӧ��
��������
���������ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ����A ����ϩ��A��������Ni�������·����ӳɷ�Ӧ����B�����飻�����������ڹ���ʱ����ȡ����Ӧ������C��һ�������HCl����ϩ��ˮ�����������£������ӳɷ�Ӧ����D���Ҵ���1��A�Ľṹ��ʽCH2===CH2��B�ṹ��ʽ��CH3CH3��C��һ������CH3CH2Cl��D���Ҵ�CH3CH2OH����2����ϩ�����������ӳɷ�Ӧ�������飬��Ӧ�ķ���ʽ�ǣ�CH2==CH2+H2![]() CH3CH3����ϩ��HCl�ڴ�������ʱ�������ӳɷ�Ӧ������һ�����飬��Ӧ�ķ���ʽ�ǣ�CH2==CH2��HCl
CH3CH3����ϩ��HCl�ڴ�������ʱ�������ӳɷ�Ӧ������һ�����飬��Ӧ�ķ���ʽ�ǣ�CH2==CH2��HCl![]() CH3CH2Cl����ϩ��ˮ��ϡ�������ʱ���ڼ��������·����ӳɷ�Ӧ�����Ҵ�����Ӧ�ķ���ʽ��CH2===CH2��H2O
CH3CH2Cl����ϩ��ˮ��ϡ�������ʱ���ڼ��������·����ӳɷ�Ӧ�����Ҵ�����Ӧ�ķ���ʽ��CH2===CH2��H2O![]() CH3CH2OH���������������ڹ���ʱ����ȡ����Ӧ������һ�������HCl����Ӧ�ķ���ʽ�ǣ�CH3CH3��Cl2
CH3CH2OH���������������ڹ���ʱ����ȡ����Ӧ������һ�������HCl����Ӧ�ķ���ʽ�ǣ�CH3CH3��Cl2![]() CH3CH2Cl��HCl��
CH3CH2Cl��HCl��

 ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д� һ��һ��һ��ͨϵ�д�
һ��һ��һ��ͨϵ�д�����Ŀ����1��������һ�������Դ,��������ȡ�봢��������Դ����������о��ȵ㡣
��֪:CH4(g)+H2O(g)��CO(g)+3H2(g) ��H=+206.2 kJ��mol-1
CH4(g)+CO2(g)��2CO(g)+2H2(g) ��H=+247.4 kJ��mol-1
2H2S(g)��2H2(g)+S2(g) ��H=+169.8 kJ��mol-1
�Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ����CH4(g)��H2O(g)��Ӧ����CO2(g)��H2(g)���Ȼ�ѧ����ʽΪ ��
��2��Na2S��ˮ��Һϴ������������������һ��С�����Ƥ�������������Ƥ��������������ˮ���Ƶ�Na2S��Һ����Ч�����á���˵��ԭ�� ����д���йصĻ�ѧ����ʽ ��
��3��ij����ˮ�к���Ca2����Mg2����Na+��K+��HCO��SO��Cl��������������������ˮ���ڹ�¯���γ�ˮ������¯ˮ�������ķ�ȼ�ϣ��������ջ���¯��Σ�գ����Ҫ���������¯ˮ����
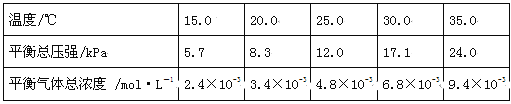
��֪��������20 ��ʱ���ܽ�����ݣ�
���� | Mg(OH)2 | CaCO3 | MgCO3 | Ca(OH)2 | CaSO4 | MgSO4 |
�ܽ��/(g/100 g H2O) | 9.0��10-4 | 1.5��10-3 | 1.0��10-2 | 1.7��10-1 | 2.1��10-1 | 26.7 |
�����û�ѧ����ʽ��ʾ��¯�е�ˮ������Mg(OH)2��ԭ��______________________��
����¯�е�ˮ�������е�CaSO4����ֱ�������ȥ����Ҫ�����Լ�X��ʹ��ת��Ϊ���������������Y����ȥ���Լ�X��________(�����)��
A.ʳ�� B.�Ȼ��� C.̼���� D.̼������
CaSO4��ת��Ϊ����Y��ԭ����(����������) _______________________________��