题目内容
【题目】(1)关于下列分子的说法不正确的是________。

A.既有σ键又有π键
B.O—H键的极性强于C—H键的极性
C.是非极性分子
D.该物质的分子之间不能形成氢键,但它可以与水分子形成氢键
(2)下列说法正确的是________。
A.HOCH2CH(OH)CH2OH与CH3CHClCH2CH3都是手性分子
B.NH![]() 和CH4的空间构型相似
和CH4的空间构型相似
C.BF3与![]() 都是平面形分子
都是平面形分子
D.CO2和H2O都是直线形分子
【答案】 CD BC
【解析】(1)A.共价单键为σ键,共价双键中含有一个σ键一个π键,该分子中含有碳碳双键,所以既有σ键又有π键,A正确;B.两种元素非金属性差距越大极性越大,O-H之间的非金属性之差大于C-H之间的非金属性之差,所以O-H键的极性强于C-H键的极性,B正确;C.结构对称,正负电荷重心重合的分子为非极性分子,该分子结构不对称,正负电荷重心不重合,所以为极性分子,C错误;D.该物质中含有酚羟基,所以该分子的分子之间能形成氢键,D错误;答案选CD;(2)A.HOCH2CH(OH)CH2OH不是手性分子,A错误;B.NH4+和CH4中中心原子价层电子对个数都是4且不含孤电子对,所以其空间构型都是正四面体结构,B正确;C.![]() 是平面型分子,BF3中B原子价层电子对个数是3且不含孤电子对,所以为平面三角形结构,C正确;D.CO2是直线形分子、H2O是V形分子,D错误;答案选BC。
是平面型分子,BF3中B原子价层电子对个数是3且不含孤电子对,所以为平面三角形结构,C正确;D.CO2是直线形分子、H2O是V形分子,D错误;答案选BC。

 名校课堂系列答案
名校课堂系列答案【题目】氯酸钾在工业上具有广泛的应用,某研究性学习小组利用如图所示的实验装置制备氯酸钾。回答下列问题:
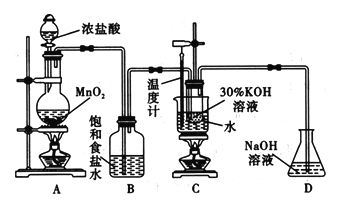
(1)写出装置C中发生反应的离子方程式:_______________________。
(2)若无B装置,则装置C中氯酸钾的产率将___________ (填“提高” “降低”或“无影响”)。
(3)在不同条件下KC1O3可将KI氧化为I2或KIO3。该小组设计了系列实验研究体系中硫酸浓度对反应产物的影响,实验的记录表如下表(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0. 20mol L-1KI/mL | V1 | 1.0 | 1.0 | 1.0 |
KC1O3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0mol L-1H2SO4/mL | 0 | 3.0 | V2 | 9.0 |
蒸馏水 | 9.0 | V3 | 3.0 | 0 |
实验现象 |
①实验设计表中V1=____________; V2 =_____________; V3 =_______________。
②设计1号试管实验的作用是_________________。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为__________________。
(4)工业上可用KC1O3与Na2SO3在H2SO4存在下制备高效、低毒的消毒剂C1O2,该反应的化学方程式为______________________ ;利用该反应原理,若工业上使用122.5吨KClO3与足量的Na2SO3反应,生成的ClO2用于除去工业废水中的Mn2+,可得到MnO2固体165吨,则该反应的产率约为___________。