题目内容
10.实验室用下面装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物.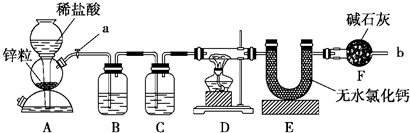
(1)如何检查装置A的气密性?关闭a,从球形漏斗口加水,待水从漏斗管上升与容器中的水面形成一段水柱,停止加水,静置片刻,如水柱不下降,证明其气密性良好
(2)装置A发生的反应有时要向其中加入少量CuSO4溶液,其目的是加快氢气产生的速率,其原理是Zn先与CuSO4反应生成Cu附着在Zn表面,Zn(负极)、Cu(正极)与稀盐酸(电解质溶液)组成很多微小原电池,发生原电池反应,加快了反应速率
(3)为了安全,在点燃D处的酒精灯之前,在b出口处必须收集氢气验纯.
(4)装置B的作用是除去氢气中的氯化氢;装置C中装的液体是浓硫酸.
(5)在气密性完好,并且进行了必要的安全操作后,点燃D处的酒精灯,在硬质双通玻璃管中发生反应的化学方程式是3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O,H2+FeO$\frac{\underline{\;高温\;}}{\;}$ Fe+H2O
(6)若FeO和Fe2O3固体混合物的质量为23.2g,反应完全后U型管的质量增加7.2g,则混合物中Fe2O3的质量为16g.
(7)U形管E右边又连接干燥管F的目的是防止空气中的水蒸气等气体进入E中,若无干燥管F,测得Fe2O3的质量将偏大(填“偏大”、“偏小”或“无影响”).
分析 (1)依据装置中气体压强变化和液面变化分析判断装置气密性;
(2)Zn先与CuSO4反应生成Cu附着在Zn表面,Zn(负极)、Cu(正极)与稀盐酸(电解质溶液)组成很多微小原电池;
(3)氢气是可燃性气体加热或点燃前需要进行验纯;
(4)A中产生的H2中混有HCl和水蒸气,必须通过洗气逐一除去,防止干扰后续实验;
(5)D装置发生的反应是氢气还原氧化亚铁、氧化铁的反应,生成了铁和水;
(6)根据氧化铁、氧化亚铁的总质量及U型管的质量增加7.2g为水的质量列式计算;
(7)若无干燥管F,空气中的水蒸气被E吸收则所测生成水的质量增大,氧元素物质的量偏大,Fe2O3的质量也将偏大.
解答 解:(1)检查装置A的气密性,需要关闭开关a,在球形漏斗中加入水到下端液面高于容器中的液面,一段时间后液面不变证明气密性完好;
故答案为:关闭a,从球形漏斗口加水,待水从漏斗管上升与容器中的水面形成一段水柱,停止加水,静置片刻,如水柱不下降,证明其气密性良好;
(2)装置A发生的反应有时要向其中加入少量CuSO4溶液,锌和硫酸铜溶液反应生成铜附着在锌表面,在稀硫酸中形成原电池反应加快反应速率,
故答案为:加快氢气产的速率;Zn先与CuSO4反应生成Cu附着在Zn表面,Zn(负极)、Cu(正极)与稀盐酸(电解质溶液)组成很多微小原电池,发生原电池反应,加快了反应速率;
(3)氢气是可燃性气体,装置中需要充满氢气后方可进行加热反应,所以需要对氢气进行验纯,避免混有空气加热发生爆炸,在F处收集氢气验纯;
故答案为:收集氢气验纯;
(4)由于A中产生的H2中混有HCl和水蒸气,必须通过洗气逐一除去,防止干扰后续实验,所以B的作用是除去氢气中的氯化氢,C的浓硫酸,用于干燥氢气,
故答案为:除去氢气中的氯化氢;浓硫酸;
(5)装置D中发生的是氧化亚铁、氧化铁与氢气的反应,反应方程式为:3H2+Fe2O32Fe+3H2O,H2+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+H2O,
故答案为:3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O,H2+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+H2O;
(6)U型管的质量增加的7.2g是水,物质的量是 $\frac{7.2g}{18g/mol}$=0.4mol,
设FeO、Fe2O3物质的量分别为X、Y,则:X+3Y=0.4
根据质量可列式:72X+160Y=23.2
解得Y=0.1,X=0.1,
所以氧化铁的质量为:160g/mol×0.1mol=16g,
故答案为:16g;
(7)干燥管F的作用防空气中水蒸气对实验干扰,若无干燥管F,空气中的水蒸气被E吸收则所测生成水的质量增大,导致氧的含量增大,Fe2O3的质量将偏大,
故答案为:防止空气中的水蒸气等气体进入E中;偏大.
点评 本题考查了测定FeO和Fe2O3固体混合物中Fe2O3的质量,是一道综合实验题,解题的关键是掌握各种装置的作用,并能根据相关的数据进行计算,此题对训练学生思维能力有一定帮助,本题难度中等.

| A. | 甲>乙>丙>丁 | B. | 丙>丁>乙>甲 | C. | 丙>丁>甲>乙 | D. | 无法判断 |
| A. | N2 | B. | O2 | C. | H2S | D. | H2 |
| A. | 三聚氰胺的摩尔质量为126g/mol | |
| B. | 三聚氰胺中C、N、H的原子个数比为1:2:2 | |
| C. | 三聚氰胺中C、N两种元素的质量比为6:7 | |
| D. | 三聚氰胺中氮元素的质量分数约为66.7% |
| A. | 标准状况下,3.36 L NO2与水充分反应转移的电子数为0.1NA | |
| B. | 12 g金刚石中含有的共价键数为4NA | |
| C. | 将22.4 L Cl2通入足量水中,反应转移的电子数为NA | |
| D. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA |
| 选项 | A | B | C | D |
| n(CO2)(mol) | 1 | 2 | 4 | 5 |
| n(沉淀)(mol) | 0 | 1 | 3 | 3 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 离子化合物中不可能含有共价键 | |
| B. | 晶体中一定存在化学键 | |
| C. | 碱性氧化物一定是金属氧化物 | |
| D. | 直径介于1-10nm之间的微粒称为胶体 |
 (1)某工厂用NH3和空气来联合处理工厂尾气中的等体积SO2和NO2,不仅除去了有害气体,还得到副产品-含两种按盐的化肥.若反应所消耗的NH3和空气的体积比为4:5(空气中O2的体积
(1)某工厂用NH3和空气来联合处理工厂尾气中的等体积SO2和NO2,不仅除去了有害气体,还得到副产品-含两种按盐的化肥.若反应所消耗的NH3和空气的体积比为4:5(空气中O2的体积