题目内容
【题目】有机物G(分子式为C13H18O2)是一种香料,下图是该香料的一种合成路线。
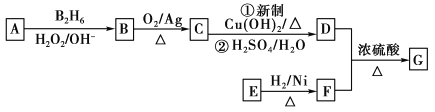
已知:
①E能够发生银镜反应,1 mol E能够与2 mol H2完全反应生成F
②R—CH=CH2![]() R—CH2CH2OH
R—CH2CH2OH
③有机物D的摩尔质量为88 g·mol-1,其核磁共振氢谱有3组峰
④有机物F是苯甲醇的同系物,苯环上只有一个无支链的侧链
回答下列问题:
(1)用系统命名法命名有机物B:__________。
(2)E的结构简式为__________。
(3)C与新制Cu(OH)2反应的化学方程式为______________________________________________。
(4)有机物C可与银氨溶液反应,配制银氨溶液的实验操作为__________________
(5)已知有机物甲符合下列条件:①为芳香族化合物②与F互为同分异构体③能被催化氧化成醛。
符合上述条件的有机物甲有_________种。其中满足苯环上有3个侧链,且核磁共振氢谱有5组峰,峰面积之比为6∶2∶2∶1∶1的有机物的结构简式为______________。
【答案】 2-甲基-1-丙醇 ![]()
![]() +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH![]()
![]() +Cu2O↓+3H2O 在一支洁净的试管中取稀AgNO3溶液少许,边振荡试管边逐滴滴加稀氨水,至产生的沉淀恰好溶解为止 13
+Cu2O↓+3H2O 在一支洁净的试管中取稀AgNO3溶液少许,边振荡试管边逐滴滴加稀氨水,至产生的沉淀恰好溶解为止 13 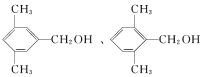
【解析】试题分析:由题中合成路线可知,B氧化为C的条件是醇的催化氧化条件,而C到D的反应条件中有醛类发生氧化的条件和酸化的条件,所以D为羧酸。又知F是苯甲醇的同系物,D和F发生酯化反应是G,由G的分子式可知,D为一元羧酸,D的相对分子质量为88,去掉1个﹣COOH剩余部分的相对质量为88﹣45=43,则![]() =3余7,则D的分子式为C4H8O2。由D的分子式并且结合G的分子式C13H18O2可知,F分子式为C9H12O。D的核磁共振氢谱显示只有3组峰,则D为(CH3)2CHCOOH,由D逆推可知C为(CH3)2CHCHO、B为(CH3)2CHCH2OH,结合信息②可知A为(CH3)2C=CH2。有机物E能够发生银镜反应,且1molE能够与2molH2完全反应生成F,且F环上只有一个无支链的侧链,则E的结构简式为
=3余7,则D的分子式为C4H8O2。由D的分子式并且结合G的分子式C13H18O2可知,F分子式为C9H12O。D的核磁共振氢谱显示只有3组峰,则D为(CH3)2CHCOOH,由D逆推可知C为(CH3)2CHCHO、B为(CH3)2CHCH2OH,结合信息②可知A为(CH3)2C=CH2。有机物E能够发生银镜反应,且1molE能够与2molH2完全反应生成F,且F环上只有一个无支链的侧链,则E的结构简式为![]() ,F为
,F为![]() ,则G为
,则G为![]() ,
,
(1)用系统命名法命名有机物B:2-甲基-1-丙醇。
(2)E的结构简式为![]() 。
。
(3)C与新制Cu(OH)2反应的化学方程式为![]() +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH![]()
![]() +Cu2O↓+3H2O。
+Cu2O↓+3H2O。
(4)有机物C可与银氨溶液反应,配制银氨溶液的实验操作为:在一支洁净的试管中加入稀AgNO3溶液少许,边振荡试管边逐滴滴加稀氨水,直至产生的沉淀恰好溶解为止 。
(5)有机物甲符合下列条件:①为芳香族化合物,说明甲分子中有苯环;②与F(![]() )互为同分异构体;③能被催化氧化成醛,说明甲分子中有羟基,且羟基的
)互为同分异构体;③能被催化氧化成醛,说明甲分子中有羟基,且羟基的![]() 至少有2个。若甲的苯环上含有1个取代基为﹣CH(CH3)CH2OH,有1种;若含有2个取代基,则可能为﹣CH2CH3和﹣CH2OH,或者﹣CH3和﹣CH2CH2OH,各有邻、间、对3种排列方式,共有6种;若含有3个取代基,则可能为﹣CH2OH和2个﹣CH3,2个﹣CH3处于邻位时,﹣CH2OH有2种位置;2个﹣CH3处于间位时,﹣CH2OH有3种位置;2个﹣CH3处于对位时,﹣CH2OH只有1种位置。综上所述,甲的结构共有13种。其中满足苯环上有3个侧链,且核磁共振氢谱有5组峰,峰面积之比为6∶2∶2∶1∶1的有机物的结构简式为
至少有2个。若甲的苯环上含有1个取代基为﹣CH(CH3)CH2OH,有1种;若含有2个取代基,则可能为﹣CH2CH3和﹣CH2OH,或者﹣CH3和﹣CH2CH2OH,各有邻、间、对3种排列方式,共有6种;若含有3个取代基,则可能为﹣CH2OH和2个﹣CH3,2个﹣CH3处于邻位时,﹣CH2OH有2种位置;2个﹣CH3处于间位时,﹣CH2OH有3种位置;2个﹣CH3处于对位时,﹣CH2OH只有1种位置。综上所述,甲的结构共有13种。其中满足苯环上有3个侧链,且核磁共振氢谱有5组峰,峰面积之比为6∶2∶2∶1∶1的有机物的结构简式为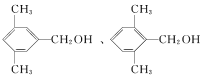 。
。

【题目】钴酸锂电池应用广泛,电池正极材料主要含有LiCoO2、导电剂乙炔黑、铝箔及少量Fe,可通过下列实验方法回收钴、锂。
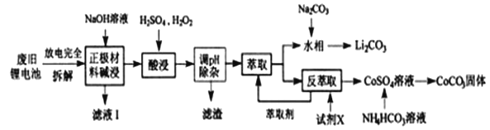
几种金属离子沉淀完全(离子浓度为10-5mo/L)的pH如下表:
离子 | Fe3+ | Al3+ | Fe2+ | Co2+ |
溶液pH | 3.2 | 4.7 | 9.0 | 9.2 |
回答下列问题:
(1)滤液I的主要成分是_________。
(2)已知:氧化性Co3+>H2O2>Fe3+,“酸浸”过程中H2O2所起主要作用是________不能用盐酸代替硫酸,原因是:__________。“调节pH”除去的离子主要有Al3+和_____。
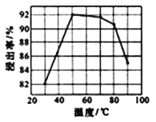
(3)酸浸时浸出率随温度变化如图所示,温度升高至50℃以上时浸出率下降的原因是_________。
(4)“萃取”和“反萃取“可简单表示为:Co2++2(HA)2![]() Co(HA2)2+2H+,则反萃取过程加入的试剂X是____________。
Co(HA2)2+2H+,则反萃取过程加入的试剂X是____________。
(5)向CoSO4溶液中加入NH4HCO3溶液,发生反应的离子方程式为_________。