题目内容
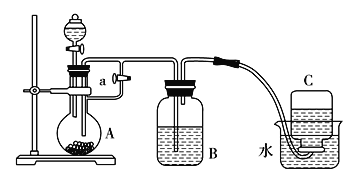
【题目】如图所示装置可用来制取Fe(OH)2并观察其在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol/L 的稀硫酸,其他试剂任选。
请完成下列问题:
(1)B装置中盛有一定量的NaOH溶液,A装置中应预先加入的试剂是________,A装置中反应的离子方程式是______________________________。
(2)实验开始时应先将活塞a________(填“打开”或“关闭”)。
(3)简述制取Fe(OH)2的操作过程:______________________________________________。
(4)实验完毕,拔去B装置中的橡胶塞,放入一部分空气,此时B装置中发生反应的化学方程式为____________________________________________。
【答案】铁屑 Fe+2H+===Fe2++H2↑ 打开 关闭活塞a,使FeSO4溶液被压入B装置中进行反应 4Fe(OH)2+2H2O+O2===4Fe(OH)3
【解析】
必须使用铁屑、6mol/L硫酸溶液制备Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化,由图可以知道,分液漏斗中为硫酸,烧瓶中为铁屑,加药品时先固体后液体,铁与硫酸反应生成硫酸亚铁和氢气,B中为NaOH溶液,实验中先打开a,利用氢气将装置中的空气排出;当关闭a时,利用氢气的压力使FeSO4溶液压入B瓶中进行反应生成Fe(OH)2,然后拔去装置B中的橡皮塞,使空气进入,可观察颜色的变化,以此来解答。
必须使用铁屑、6mol/L硫酸溶液制备Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化,由图可以知道,分液漏斗中为硫酸,烧瓶中为铁屑,加药品时先固体后液体,铁与硫酸反应生成硫酸亚铁和氢气,B中为NaOH溶液,
(1)A中应预先加入的试剂是铁屑,A中发生的反应的离子方程式为Fe+2H+===Fe2++H2↑,
因此,本题正确答案是:铁屑;Fe+2H+===Fe2++H2↑;
(2)实验开始时应先将活塞a打开,其目的是排出B中的空气,
因此,本题正确答案是:打开;
(3)生成Fe(OH)2的操作过程为关闭活塞a,A中压强增大,将FeSO4溶液压入B瓶中进行反应,
因此,本题正确答案是:关闭活塞a,使FeSO4溶液被压入B装置中进行反应;
(4)拔去装置B中的橡皮塞,使空气进入,看到的现象为白色沉淀迅速变成灰绿色,最后变成红褐色,发生的反应为4Fe(OH)2+2H2O+O2===4Fe(OH)3,
因此,本题正确答案是:4Fe(OH)2+2H2O+O2===4Fe(OH)3。

 阅读快车系列答案
阅读快车系列答案