题目内容
【题目】丙烯是重要的有机化工原料,丙烷脱氢制丙烯具有显著的经济价值和社会意义。回答下列问题。
(1)已知:I.2C3H8(g)+O2(g)=2C3H6(g)+2H2O(g) ΔH=-238kJ·mol-1
II.2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ·mol-1
则丙烷脱氢制丙烯反应C3H8(g)![]() C3H6(g)+H2(g)的ΔH为___。
C3H6(g)+H2(g)的ΔH为___。
(2)如图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分别为104Pa和105Pa)。
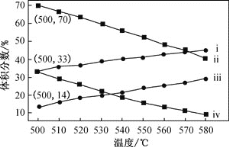
104Pa时,图中表示丙烯的曲线是__(填“ⅰ”、“ⅱ”、“ⅲ”或“ⅳ”)。
(3)一定温度下,向恒容密闭容器中充入1molC3H8,开始压强为pkPa,发生丙烷脱氢制丙烯反应。
①下列情况能说明丙烷脱氢制丙烯反应达到平衡状态的是__(填字母)。
A.该反应的焓变(ΔH)保持不变
B.气体平均摩尔质量保持不变
C.气体密度保持不变
D.C3H8分解速率与C3H6消耗速率相等
②欲使丙烯的平衡产率提高,应采取的措施是__(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
③为提供反应所需热量,恒压时若向原料气中掺入水蒸气,则丙烷脱氢反应的K__(填“增大”、“减小”或“不变”)
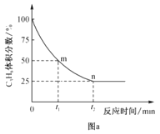
(4)丙烷脱氢制丙烯反应过程中,C3H8的气体体积分数与反应时间的关系如图a所示。此温度下该反应的平衡常数Kp=__kPa(用含字母p的代数式表示,Kp是用反应体系中气体物质的分压表示的平衡常数,平衡分压=总压×物质的量分数)。
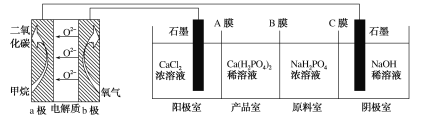
(5)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图。
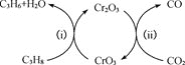
图中催化剂为__。该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是__。
【答案】+123kJ/mol i BD AD 增大 0.9P CrO3 C与CO2反应生成CO,脱离催化剂表面
【解析】
根据已知热化学方程式和盖斯定律进行计算;结合压强越大平衡逆向进行,丙烯体积分数越小判断丙烯的代表曲线;根据“变量”可作为达到平衡的标志进行分析判断;根据达到平衡时,丙烷的体积分数为25%,列出三段式计算平衡时各气体的物质的量分数,进而计算分压,再计算Kp。
(1)已知热化学方程式:I.2C3H8(g)+O2(g)=2C3H6(g)+2H2O(g) H=-238kJ·mol-1,II.2H2(g)+O2(g)=2H2O(g) H=-484kJ·mol-1,根据盖斯定律可知,![]() (I-II)可得目标方程式C3H8(g)
(I-II)可得目标方程式C3H8(g)![]() C3H6(g)+H2(g),则
C3H6(g)+H2(g),则![]() ,故答案为:+123kJ/mol;
,故答案为:+123kJ/mol;
(2)C3H8(g)![]() C3H6(g)+H2(g),△H1=+124.3kJ/mol,温度越高丙烯的体积分数越大;压强越大平衡逆向进行,丙烯体积分数越小,丙烯是生成物,减压过程中体积分数增大,由此判断图中表示丙烯的曲线是i,故答案为i;
C3H6(g)+H2(g),△H1=+124.3kJ/mol,温度越高丙烯的体积分数越大;压强越大平衡逆向进行,丙烯体积分数越小,丙烯是生成物,减压过程中体积分数增大,由此判断图中表示丙烯的曲线是i,故答案为i;
(3)①容器的容积不变,该反应C3H8(g)![]() C3H6(g)+H2(g)的正反应为气体物质的量增大的反应。
C3H6(g)+H2(g)的正反应为气体物质的量增大的反应。
A.该反应的焓变(H)为一定值,无论反应是否达到平衡,始终保持不变,则该反应的焓变(H)保持不变,不能说明反应达到平衡状态,故A不符合;
B.混合气体的总质量不变,随着反应的进行,气体物质的量增大,则气体平均摩尔质量会减小,则当气体平均摩尔质量保持不变时,能说明反应达到平衡状态,故B符合;
C.混合气体的总质量不变,容器的容积不变,则气体密度为一定值,始终保持不变,则气体密度保持不变,不能说明反应达到平衡状态,故C不符合;
D.C3H8的分解速率为正反应速率,C3H6的消耗速率为逆反应速率,二者相等,则C3H8的分解速率与C3H8的生成速率相等,说明正逆反应速率相等,能说明反应达到平衡状态,故D符合;
故答案为:BD;
②反应C3H8(g)![]() C3H6(g)+H2(g)△H1=+124.3kJ/mol,正反应为吸热反应,反应前后体积增大,可采用升高温度和降低压强的方法使丙烯的平衡产率提高,故答案为:AD;
C3H6(g)+H2(g)△H1=+124.3kJ/mol,正反应为吸热反应,反应前后体积增大,可采用升高温度和降低压强的方法使丙烯的平衡产率提高,故答案为:AD;
③恒压时若向原料气中掺入水蒸气,反应温度升高,平衡正向移动,丙烷脱氢反应的平衡常数K增大,故答案为:增大;
(4)由图可知达到平衡时,丙烷的体积分数为25%,设丙烷的转化量为xmol,可列出三段式
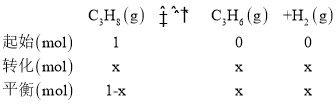
则丙烷的体积分数为![]() ,解得x=0.6,则平衡时气体总物质的量为1.6mol,根据恒温恒容时,压强之比等于物质的量之比可得,平衡时,气体的总压强为1.6pkPa,丙烯的物质的量分数、氢气的物质的量分数均为
,解得x=0.6,则平衡时气体总物质的量为1.6mol,根据恒温恒容时,压强之比等于物质的量之比可得,平衡时,气体的总压强为1.6pkPa,丙烯的物质的量分数、氢气的物质的量分数均为![]() ,则p(C3H8)=
,则p(C3H8)=![]() ,p(C3H6)=p(H2)=
,p(C3H6)=p(H2)=![]() ,则
,则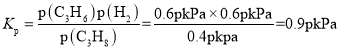 ,故答案为:0.9P;
,故答案为:0.9P;
(5)根据图示可知,该工艺中CrO3作催化剂时,碳与CO2反应生成CO,可以有效消除催化剂表面的积炭,维持催化剂活性,故答案为:CrO3;C与CO2反应生成CO,脱离催化剂表面。

【题目】化学小组探究铜与硝酸反应的快慢及产物。
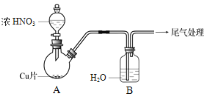
(1)实验甲:将铜片放入盛有稀HNO3的试管中,开始无明显现象,后逐渐有小气泡生成,该气体是______。在液面上方出现浅红棕色气体,溶液呈蓝色。
(2)实验乙:铜与浓HNO3反应,装置、现象如下:
实验装置 | 实验现象 |
| A中:最初反应较慢,随后加快,反应剧烈;产生红棕色气体;溶液呈绿色。 B中:溶液呈淡蓝色。 |
①A中铜与浓HNO3产生红棕色气体的化学方程式是 ______。
②实验现象“最初反应较慢,随后加快”的原因可能是 ______。
(3)有文献记载:铜与浓HNO3反应一旦发生就变快,是因为开始生成的NO2溶于水形成HNO2(弱酸,不稳定),它再和Cu反应,反应就加快。实验探究如下:
I:向 1 mL浓硝酸中加入几滴30% H2O2溶液、铜片,反应较慢,溶液呈蓝色。
II:向1 mL浓硝酸中加入几滴30% H2O2溶液,无明显变化。
①I中反应变慢的原因是 ______。
②NO2与H2O反应生成HNO2和 ______。
③对生成HNO2后反应变快的原因进行实验探究。
序号 | 实验操作 | 实验现象 |
III | 取B中溶液,加入一定量固体,再加入铜片 | 立即产生无色气体;液面上方呈红棕色 |
IV | 取B中溶液,放置一段时间,溶液变为无色后,再加入铜片 | 产生无色气体,较Ⅲ慢;液面上方呈浅红棕色 |
a.III中加入的固体为______。
b.IV中“放置一段时间”的目的是 ______。
实验III、IV可以说明,HNO2氧化Cu的反应速率比HNO3氧化Cu的反应快。
(4)化学小组同学结合实验甲、乙中HNO3被还原后的气体产物以及实验III的产物,综合上述实验,分析判断甲中反应慢的原因,除了硝酸起始浓度小、反应过程中温度较低外,另一个重要原因是 ______。
【题目】为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。
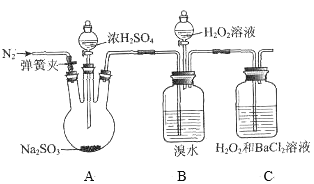
实验操作 | 实验现象 |
ⅰ.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
ⅱ.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
ⅲ.打开B中分流漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)A中发生反应的化学方程式是____。
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是____。
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是___。
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性H2O2>SO2。
(3)ⅲ中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br―
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是________。
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是____。