题目内容
【题目】设NA表示阿伏加德罗常数的值,下列说法错误的是( )
A.1mol的Fe分别与足量的盐酸和稀硫酸反应,电子转移数目均为2NA
B.125gCuSO4·5H2O晶体中含有0.5NA个Cu2+
C.常温常压下,等质量的SO2、S2含有相同的分子数
D.1molNa2O2固体中含原子总数为3NA
【答案】D
【解析】
A.铁和盐酸反应生成氯化亚铁和氢气,1mol Fe与足量的盐酸反应电子转移总数为2NA,1molFe与足量稀硫酸反应时生成1mol硫酸亚铁,转移电子数为2NA,故A正确;
B.CuSO45H2O中n(Cu2+)=n(CuSO45H2O),125gCuSO45H2O的物质的量为![]() =0.5mol,含有0.5NA个Cu2+,故B正确;
=0.5mol,含有0.5NA个Cu2+,故B正确;
C.SO2、S2的摩尔质量相同,等质量的SO2、S2具有相同的物质的量,具有相同的分子数,故C正确;
D.过氧化钠是由两个钠离子和一个过氧根离子构成,1molNa2O2固体中含离子总数为3NA,原子总数为4NA,故D错误;
故选D。

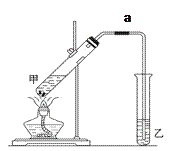
【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);

有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | 33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)甲装置中仪器A的名称为_______。
(2)用甲装置制氯气,MnO4 被还原为Mn2+,该反应的离子方程式为________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到_______(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:
①促进氯气与锡反应;②__________。
(4)如果缺少乙装置,丁装置中可能产生SnCl2杂质,产生SnCl2杂质的化学方程式为______,以下试剂中可用于检测是否产生SnCl2的有_____
A.H2O2溶液 B.FeCl3溶液(滴有KSCN) C.AgNO3溶液 D.溴水
(5)己装置的作用是_____。
A.除去未反应的氯气,防止污染空气
B.防止空气中CO2气体进入戊装置
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O2进入戊装置的试管中使产物氧化
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.35gSnCl4,则SnCl4的产率为____(保留3位有效数字)。