题目内容
(10分)AB2离子化合物的阴、阳离子的电子层结构相同,每摩尔AB2分子中含有54mol电子,根据下列反应:
① H2+ B2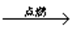 C ② B2 + X → Y + AB2 + H2O
C ② B2 + X → Y + AB2 + H2O
③ Y+C → AB2 + Z(Z有漂白作用)
(1)写出下列物质的化学式:AB2________,X_________,Y_________
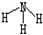
(2)用电子式表示AB2的形成过程____________
(3)写出反应②的化学方程式____________
① H2+ B2
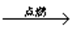 C ② B2 + X → Y + AB2 + H2O
C ② B2 + X → Y + AB2 + H2O ③ Y+C → AB2 + Z(Z有漂白作用)
(1)写出下列物质的化学式:AB2________,X_________,Y_________
(2)用电子式表示AB2的形成过程____________
(3)写出反应②的化学方程式____________
(1)CaCl2 Ca(OH)2 Ca(ClO)2
(2)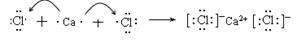
(3)Ca(OH)2+2Cl2=CaCl2+ Ca(ClO)2+H2O
(2)
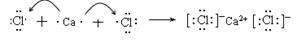
(3)Ca(OH)2+2Cl2=CaCl2+ Ca(ClO)2+H2O
AB2离子化合物的阴、阳离子的电子层结构相同,因此阴阳离子的电子数相同。又因为每摩尔AB2分子中含有54mol电子,所以1个离子中含有的电子数是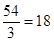 。根据化合物的化学式可知A是钙元素,B是氯元素,即化合物是CaCl2,属于由离子键构成的离子化合物。根据转化关系式①可判断,C是氯化氢。Z具有漂白作用,所以根据③可知Y是Ca(ClO)2,Z是HClO。因此根据②可判断,X是Ca(OH)2。
。根据化合物的化学式可知A是钙元素,B是氯元素,即化合物是CaCl2,属于由离子键构成的离子化合物。根据转化关系式①可判断,C是氯化氢。Z具有漂白作用,所以根据③可知Y是Ca(ClO)2,Z是HClO。因此根据②可判断,X是Ca(OH)2。
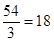 。根据化合物的化学式可知A是钙元素,B是氯元素,即化合物是CaCl2,属于由离子键构成的离子化合物。根据转化关系式①可判断,C是氯化氢。Z具有漂白作用,所以根据③可知Y是Ca(ClO)2,Z是HClO。因此根据②可判断,X是Ca(OH)2。
。根据化合物的化学式可知A是钙元素,B是氯元素,即化合物是CaCl2,属于由离子键构成的离子化合物。根据转化关系式①可判断,C是氯化氢。Z具有漂白作用,所以根据③可知Y是Ca(ClO)2,Z是HClO。因此根据②可判断,X是Ca(OH)2。
练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目