题目内容
我国成功研制的铯(133Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提高到600万年不差1秒。已知该铯原子的核外电子数为55,则该原子的中子数为( )
| A.23 | B.55 | C.78 | D.133 |
C
考查原子的组成及表示方法。在表示原子组成时,元素符号的左下角表示的是质子数,左上角表示的是质量数。质子数和中子数之和是质量数,质子数等于核外电子数,所以该原子的中子数是133-55=78,答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
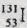 ,下列有关
,下列有关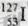 相同
相同 C ② B2 + X → Y + AB2 + H2O
C ② B2 + X → Y + AB2 + H2O 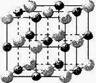
 Hf。下列关于
Hf。下列关于