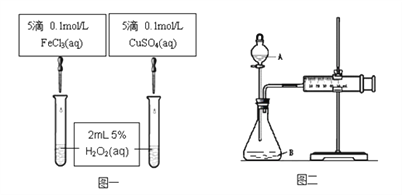
��Ŀ����
����Ŀ����ѧ��һֱ�����ڡ��˹��̵����ķ����о���
��1��Ŀǰ�ϳɰ��ļ���ԭ��Ϊ��N2(g)+3H2(g) 2NH3(g) ��H �÷�Ӧ�������仯��ͼ��ʾ��
2NH3(g) ��H �÷�Ӧ�������仯��ͼ��ʾ��

���ڷ�Ӧ��ϵ�м����������Ӧ��������E2�ı仯�ǣ�______________�������������С�����䡱����
�ڽ�һ������N2(g)��H2(g)����2L���ܱ������У���500�桢2��107Pa�·������·�Ӧ��![]()
5���Ӻ�ﵽƽ�⣬���N2Ϊ0.2 mol��H2Ϊ0.6 mol��NH3Ϊ0.2 mol��������ƽ����Ӧ����v(N2)��_______________��H2��ת����Ϊ_______________���÷�Ӧ�ڴ��¶��µĻ�ѧƽ�ⳣ��Ϊ_______________���������ձ���С�����һλ��
������ߢ�������H2��ת���ʣ����д�ʩ���е���____________��
A���������а�ԭ�����ٳ���ԭ����
B�����������ٳ����������
C���ı䷴Ӧ�Ĵ���
D��Һ��������������
��2��1998��ϣ������ʿ��´�ѧ����λ��ѧ�Ҳ��ø����ӵ����Ե�SCY�մɣ��ܴ���H+�����Ӷ�ʵ���˸�ת���ʵĵ�ⷨ�ϳɰ�����ʵ��װ����ͼ��ʾ�������ĵ缫��ӦʽΪ_____________________��

��3���������¡��˹��̵������о��������ڳ��¡���ѹ�����������£�N2�ڴ�������������Fe2O3��TiO2��������ˮ�������з�Ӧ��
2N2(g) +6H2O(l) ![]() 4NH3(g) +3O2(g) ��H = a kJ/mol
4NH3(g) +3O2(g) ��H = a kJ/mol
��һ���о�NH3���������¶ȹ�ϵ����ѹ�´ﵽƽ��ʱ��ò���ʵ���������£�
T/K | 303 | 313 | 323 |
NH3������/��10��6mol�� | 4.8 | 5.9 | 6.0 |
�˺ϳɷ�Ӧ��a_________0��������ڡ�����С�ڡ����ڡ���
���𰸡���С0.01mol��L��1��min��133.3%3.7 L2/mol2A DN2 + 6H+ + 6e�� = 2NH3����
��������
�����������1����������������ͷ�Ӧ�Ļ�ܣ�
����������ʽ���㣻
���������������ƽ��״̬��Ӱ�������
��2���������������õ����ӵĻ�ԭ��Ӧ��
��3�������¶������������֮��Ĺ�ϵ�жϡ�
��������1����������������ͷ�Ӧ�Ļ�ܣ���E1��E2����С��
�� ![]()
��ʼŨ�ȣ�mol/L�� 0.15 0.45 0
ת��Ũ�ȣ�mol/L�� 0.05 0.15 0.1
ƽ��Ũ�ȣ�mol/L�� 0.1 0.3 0.1
����������ƽ����Ӧ����v(N2)��0.05mol/L��5min��0.01mol/(L��min)��H2��ת����Ϊ![]() ���÷�Ӧ�ڴ��¶��µĻ�ѧƽ�ⳣ��Ϊ
���÷�Ӧ�ڴ��¶��µĻ�ѧƽ�ⳣ��Ϊ![]() ��
��
��A���������а�ԭ�����ٳ���ԭ�����൱������ѹǿ��ƽ��������Ӧ������У�ת������ߣ�A��ȷ��B�����������ٳ����������Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���ת���ʲ��䣬B����C���ı䷴Ӧ�Ĵ������ܸı�ƽ��״̬��ת���ʲ��䣬C����D��Һ��������������������������Ũ�ȣ�ƽ��������Ӧ������У�ת������ߣ�D��ȷ����ѡAD��
��2�����ص������õ����ӣ������������õ����ӣ�������ԭ��Ӧת��Ϊ�������缫��ӦʽΪN2 + 6H+ + 6e����2NH3��
��3�����ݱ������ݿ�֪�����¶Ȱ����������ӣ�˵�������¶�ƽ��������Ӧ������У�����Ӧ�����ȷ�Ӧ����a��0��