题目内容
18.在t℃下,某反应达到平衡,平衡常数K=$\frac{c(NO)c(S{O}_{3})}{c(N{O}_{2})c(S{O}_{2})}$.恒容时,温度升高,NO浓度减小.下列说法正确的是( )| A. | 该反应的焓变为正值 | |
| B. | K表达式中,C(SO3)指反应在该条件下达到化学平衡时SO3的物质的量浓度 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应化学方程式为:NO+SO3?NO2+SO2 |
分析 平衡常数K=$\frac{c(NO)•c(S{O}_{3})}{c(N{O}_{2})•c(S{O}_{2})}$.反应的化学方程式为NO2+SO2=NO+SO3恒容时,升高温度,NO浓度减小,说明平衡逆向进行,依据平衡移动原理和影响反应速率的因素分析选项;
A、NO2+SO2=NO+SO3,恒容时,升高温度,NO浓度减小,说明平衡逆向进行,逆反应为吸热反应,正反应为放热反应,焓变为负值;
B、化学平衡常数表达式中的浓度是指平衡时的浓度;
C、升温正逆反应速率 都增大;
D、依据化学平衡常数可知,NO、SO3为生成物,NO2、SO2为反应物,以此书写化学方程式.
解答 解:A、恒容时,升高温度,NO浓度减小,说明平衡逆向进行,逆反应为吸热反应,正反应为放热反应,焓变为负值,故A错误;
B、化学平衡常数表达式中的浓度是指平衡时的浓度,所以K表达式中,C(SO3)指反应在该条件下达到化学平衡时SO3的物质的量浓度,故B正确;
C、升温反应速率增大,正逆反应速率都增大,故C错误;
D、依据化学平衡常数概念书写化学方程式为NO2+SO2=NO+SO3,故D错误;
故选B.
点评 本题考查了化学平衡常数概念分析,平衡常数和反应速率影响因素分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
8.下列说法中一定正确的是( )
| A. | pH=7的溶液中性 | B. | pH>7,溶液呈碱性 | ||
| C. | pH=6溶液中[OH-]=1×10-8 mol•L-1 | D. | pH=6溶液中[H+]=1×10-6 mol•L-1 |
9.下列各组物质,仅用蒸馏水不能鉴别的是( )
| A. | 氧化铜、二氧化锰、活性炭 | B. | 汽油、酒精、四氯化碳 | ||
| C. | 食盐、烧碱、硝酸铵 | D. | 蔗糖、硫酸铜粉末、碳酸钙 |
6.往FeCl3和BaCl2的混合溶液中通入SO2,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生.下列说法不正确的是( )
| A. | 该实验表明SO2有漂白性 | B. | 白色沉淀为BaSO4 | ||
| C. | 该实验表明FeCl3有氧化性 | D. | 反应后溶液酸性增强 |
13.下列各组中两种气体分子数一定相等的是( )
| A. | 温度相等、体积相同的O2和N2 | B. | 质量相等、密度不等的N2和C2H4 | ||
| C. | 体积相等、密度相等的CO和O2 | D. | 压强相等、体积相同的N2O和CO2 |
3.金属钠分别与下列溶液反应时,既有沉淀析出,又有气体逸出的是( )
| A. | BaCl2溶液 | B. | K2SO4溶液 | C. | CuSO4 | D. | NH4NO3溶液 |
10.一定温度下,某密闭容器中的反应为:aX(g)+bY(g))?cZ(g)+dW(g),经5min达到平衡,X减少n mol/L,Y减少n/3mol/L,Z增加2n/3mol/L.若将体系压强增大,W的百分含量不发生变化,则a:b:c:d为( )
| A. | 3:1:2:1 | B. | 1:3:2:2 | C. | 1:3:1:2 | D. | 3:1:2:2 |
7.2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉的婴幼儿产生肾结石病症,其原因是奶粉中含有三聚氰胺.三聚氰胺的分子式为C3N3(NH2)3,在一般情况下较稳定,但在高温下可能会分解放出氰化物.下列有关三聚氰胺的说法不正确的是( )
| A. | 三聚氰胺的摩尔质量为126 | |
| B. | 用三聚氰胺制造的餐具不可以放进微波炉中加热使用 | |
| C. | 三聚氰胺中C、N两种元素的质量比为3:7 | |
| D. | 三聚氰胺中氮元素的质量分数约为66.7% |
8.已知有机物A的红外光谱和核磁共振氢谱如图,下列说法错误的是( )
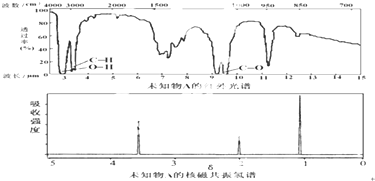

| A. | 由红外光谱可知,该有机物中至少有三种不同的化学键 | |
| B. | 由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子 | |
| C. | 仅由其核磁共振氢谱无法得知其分子中的氢原子总数 | |
| D. | 若A的化学式为C3H6O,则其结构简式为CH3COCH3 |