题目内容
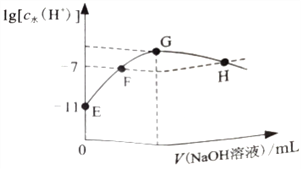
【题目】常温下,在新制氯水中滴加NaOH 溶液,溶液中水电离出来的c水(H+)的对数与NaOH 溶液体积之间的关系如图所示。下列推断正确的是
A. 用pH试纸测定E点对应的溶液,其pH=3
B. F、H点对应的溶液中都存在c(Na+)=c(Cl-)+c(ClO-)
C. 加水稀释H点对应的溶液,溶液的pH增大
D. G点对应的溶液中c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+)
【答案】D
【解析】A. E点溶液为氯水,具有漂白性,pH试纸褪色,不能用pH试纸测定E点对应的溶液的pH,故A错误;B.根据电荷守恒,c(Na+)+ c(H+)=c(Cl-)+c(ClO-)+ c(OH-),F溶液中含有次氯酸钠、氯化钠和次氯酸,H点溶液中含有次氯酸钠、氯化钠和氢氧化钠,尽管溶液中由水电离的c(H+)相等,但溶液中溶质的浓度不等,溶液的pH不等,因此c(H+)≠ c(OH-),F点为中性,H点为碱性,因此H点溶液中不存在c(Na+)=c(Cl-)+c(ClO-),故B错误;C. 加水稀释H点对应的溶液,溶液的碱性减弱,pH减小,故C错误;D. G点对应的溶液为次氯酸钠溶液和氯化钠,且物质的量浓度相等,水的电离程度最大,次氯酸钠水解,溶液显碱性, c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+),故D正确;故选D。

【题目】表是25℃时四种酸的电离平衡常数:
化学式 | CH3COOH | HA | HNO2 | H2CO3 |
Ka | Ka=1.8×10﹣5 | Ka=4.9×10﹣10 | Ka=4.6×10﹣4 | Ka1 =4.1×10﹣7 |
(1)用离子方程式表示NaNO2溶液呈碱性的原因
(2)25℃时,向向0.1molL﹣1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO﹣)=5:9,此时溶液pH=
(3)写出NaA溶液中通少量CO2的离子方程式
(4)25℃时,等物质的量浓度的HA、NaA混合溶液呈碱性,溶液中各离子浓度的大小顺序为
(5)已知HNO2不稳定,在稀溶液中也易分解生成NO与NO2 , 某同学分别取少量NaCl溶液与NaNO2溶液于试管中,分别滴加浓醋酸,以此来鉴别失去标签的NaCl溶液和NaNO2溶液,该方法(填“可行”或“不可行”),理由是
(6)已知NaHCO3溶液中存在HCO3H++CO32﹣ , 加水稀释时溶液中的c(H+)将(填“增大”或“减小”)
