题目内容
8. CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:
CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:(1)一定温度下,在一体积为VL的密闭容器中充人一定量的NO和CO时,反应进行到t时刻时达到平衡状态,此时n(CO)=amol、n(N0)=2amol、n(N2)=bmol,且N2占平衡混合气体总体积的$\frac{1}{4}$.
①该反应的平衡常数K=$\frac{27}{aV}$(用只含a、V的式子表示)
②判断该反应达到平衡的标志是BD(填序号)
A.v(CO2)生成=v(CO)消耗
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
D.NO、CO、N2、CO2的物质的量浓度均不再变化
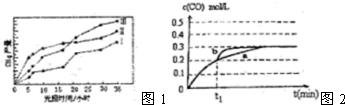
(2)在一定温度下,将2.0molNO、2.4molCO通入固定容积2L的密闭中,反应过程中部分物质的物质的量变化如图所示,则:
①有害气体NO的转化率是40%,0~15minCO2的平均反应速率v(CO2)=0.027mol(L.min).(保留小数点后三位)
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件是CD.(填序号).
A.增加CO的量 B.加入催化剂C.减小CO2的量 D.扩大容器体积.
分析 (1)①平衡时n(CO)=amol、n(NO)=2amol、n(N2)=bmol,则根据方程式可知生成CO2是2bmol.又因为N2占平衡混合气体总体积的$\frac{1}{4}$,所以平衡时混合气体的总的物质的量是4b mol,则4bmol=bmol+2bmol+amol+2amol,解得b=3a,再由平衡常数表达式K=$\frac{c({N}_{2})×{c}^{2}(C{O}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$计算;
②可逆反应到达平衡时,正逆反应速率相等,反应各组分的浓度、含量不变,由此衍生的其它物理量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化,说明到达平衡;
(2)①发生反应:2NO+2CO=N2+2CO2,计算消耗CO物质的量,根据方程式计算消耗NO物质的量,进而计算NO转化率;根据v=$\frac{△c}{△t}$计算v(N2),再利用速率之比等于化学计量数之比计算v(CO2);
②20min时,若改变反应条件,导致CO浓度减小,可以使平衡向正反应方向移动,不能增大CO浓度、不能增大压强,否则到达平衡时CO浓度会增大,也可以扩大容器体积.
解答 解:(1)①平衡时n(CO)=amol、n(NO)=2amol、n(N2)=bmol,则根据方程式可知生成CO2是2bmol.又因为N2占平衡混合气体总体积的$\frac{1}{4}$,所以平衡时混合气体的总的物质的量是4b mol,则4bmol=bmol+2bmol+amol+2amol,解得b=3a,平衡常数K=$\frac{c({N}_{2})×{c}^{2}(C{O}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$=$\frac{\frac{3a}{V}×(\frac{6a}{V})^{2}}{(\frac{2a}{V})^{2}×(\frac{a}{V})^{2}}$=$\frac{27V}{a}$,
故答案为:$\frac{27V}{a}$;
②A.v(CO2)生成=v(CO)消耗,均表示正反应速率,所以不能说明反应达到平衡状态,故A错误;
B.混合气体总质量不变,但物质的量是变化的,因此混合气体的平均相对分子质量不再改变可以说明反应达到平衡状态,故B正确;
C.在反应过程中气体总质量和容积始终是不变的,因此密度始终是不变的,则混合气体的密度不再改变不能说明反应达到平衡状态,故C错误;
D.NO、CO、N2、CO2的物质的量浓度均不再变化,说明正逆反应速率相等,反应达到平衡状态,故D正确,
故选:BD;
(2)①发生反应:2NO+2CO=N2+2CO2,平衡时CO是1.6mol,则消耗CO是2.4mol-1.6mol=0.8mol,根据方程式可知消耗NO是0.8mol,因此有害气体NO的转化率是$\frac{0.8mol}{2.0mol}$×100%=40%,
v(N2)=$\frac{\frac{0.4mol}{2L}}{15min}$=$\frac{1}{75}$mol/(L.min),速率之比等于化学计量数之比,v(CO2)=2v(N2)=2×$\frac{1}{75}$mol/(L.min)=0.027mol/(L.min),
故答案为:40%;0.027mol/(L.min);
②A.增加CO的量,CO浓度增大,故A错误;
B.加入催化剂平衡不移动,CO浓度不变,故B错误;
C.减小CO2的量,平衡向正反应方向进行,CO浓度减小,故C正确;
D.扩大容积体积,压强减小,平衡虽然向逆反应方向进行,但平衡常数不变,CO浓度仍然减小,故D正确,
故选:CD.
点评 本题考查化学平衡有关计算、平衡状态判断、以及外界条件对平衡状态的影响等,是对学生综合能力的考查,难度中等.

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
(已知:AlO2-+H++H2O=Al(OH)3↓)

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有3类.
(2)步骤①中涉及SiO2的离子反应方程式为SiO2+2OH-=SiO32-+H2O.
(3)滤渣A的成分有Fe2O3填化学式)
(4)步骤②洗涤时,检验是否洗涤干净的方法是?:取最后一次洗涤滤液,加硝酸银溶液,若无沉淀产生,则说明洗涤干净
(5)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+SiO2;实验室进行步骤③用到的仪器有坩埚钳、酒精灯、三脚架、坩埚和泥三角.
 已知NH3是能用来做喷泉实验的气体,若在同温同压下用等体积烧瓶一个收集满NH3,另一个收集NH3和N2的混合气体,如图所示,喷泉实验停止后,两个烧瓶内溶液的关系式(不考虑烧瓶内溶质的扩散,氯水的溶质按NH3计算)( )
已知NH3是能用来做喷泉实验的气体,若在同温同压下用等体积烧瓶一个收集满NH3,另一个收集NH3和N2的混合气体,如图所示,喷泉实验停止后,两个烧瓶内溶液的关系式(不考虑烧瓶内溶质的扩散,氯水的溶质按NH3计算)( )| A. | 溶质的物质的量浓度相同,溶质的质量分数不同 | |
| B. | 溶质的质量分数相同,溶质的物质的量不同 | |
| C. | 溶质的物质的量浓度和溶质的质量分数都不同 | |
| D. | 溶质的物质的量浓度和溶质的质量分数都相同 |
| A. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| B. | 某物质的溶液pH<7,则该物质一定是酸 | |
| C. | pH=7的某溶液一定呈中性 | |
| D. | pH=7.6的氨水,c(H+)>10-7mol/L |