题目内容
硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发达水平的一种标志。目前主要生产方法是“接触法”,有关2SO2+O2 2SO3的说法中,不正确的是
2SO3的说法中,不正确的是
 2SO3的说法中,不正确的是
2SO3的说法中,不正确的是 | A.该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3 |
| B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零 |
| C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻之后,正、逆反应速率相等 |
| D.平衡时SO2、O2、SO3的分子数之比不再改变 |
B
试题分析:A、可逆反应是在一定条件下不能进行彻底的反应,正反应和逆反应同时进行,该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3 ,故A正确;B、达到平衡后,正反应速率和逆反应速率相同,是动态平衡,速率不能为0,故B错误;C、一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等达到平衡,故C正确;D、平衡时各种物质的浓度不再发生变化,所以平衡时SO2、O2、SO3的分子数之比不再改变,故D正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题,试题针对性强,注重基础,侧重对学生能力的培养,有利于培养学生的逻辑推理能力和抽象思维能力。理解并掌握平衡的可逆性是解题关键。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 aZ(g) △H=QkJ·mol-1,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图像,下列有关说法正确的是
aZ(g) △H=QkJ·mol-1,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图像,下列有关说法正确的是
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据: (4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为: 和 。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为 。(Li的相对原子质量约为7.0)
(4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为: 和 。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为 。(Li的相对原子质量约为7.0) 2C(g)若经2 s 后测得C的浓度为0.6 mol/L,下列几种说法正确的是:①用物质A表示的反应的平均速率为0.3 mol/(L·s);②用物质B表示的反应的平均速率为0.6 mol/(L·s);③反应达到平衡时,A、B、C的反应速率一定相等;④反应达到平衡时,A、B、C的物质的量均不再变化
2C(g)若经2 s 后测得C的浓度为0.6 mol/L,下列几种说法正确的是:①用物质A表示的反应的平均速率为0.3 mol/(L·s);②用物质B表示的反应的平均速率为0.6 mol/(L·s);③反应达到平衡时,A、B、C的反应速率一定相等;④反应达到平衡时,A、B、C的物质的量均不再变化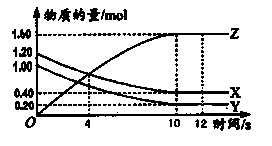
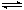 2Z
2Z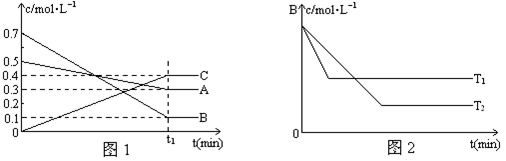
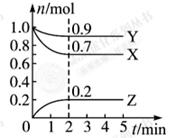
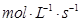 与用物质Y表示的化学反应速率为0.1
与用物质Y表示的化学反应速率为0.1 2SO3(g)。反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol。
2SO3(g)。反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol。