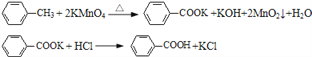
题目内容
【题目】如图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( )

A. 此过程中没有分解反应
B. 整个过程的反应可表示为: 2SO2+2CaCO3+O2═2CaSO4+2CO2
C. 使用此废气处理装置可减少CO2的排放
D. 此过程中S元素的化合价未发生改变
【答案】B
【解析】A.转化中碳酸钙分解能生成氧化钙和二氧化碳;B.整个过程中,二氧化硫与碳酸钙和氧气反应生成了硫酸钙和二氧化碳;C.整个过程中,二氧化硫与碳酸钙和氧气反应生成了硫酸钙和二氧化碳, 2SO2+2CaCO3+O2═2CaSO4+2CO2;D.亚硫酸钙中,硫元素的化合价是+4,硫酸钙中,硫元素的化合价是+6。
碳酸钙分解生成氧化钙,此反应方程式为CaCO3=CaO+CO2↑,属于分解反应,A错误;由于此废气处理装置中进入反应器中的物质有:CaCO3、SO2、空气(其中O2参与反应),排出的物质有:CaSO4、CO2,故反应方程式为:2SO2+2CaCO3+O2═2CaSO4+2CO2; B正确;该装置是将SO2气体转化成CO2,增加了CO2的排放,减少了SO2的排放,C错误;此过程中进入装置的气体为SO2,硫的化合价为+4价,而排出为CaSO4,硫的化合价为+6价,则硫的化合价发生了变化,D错误;正确选项B。

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目